发布时间:2022/08/22 点击数:
发布时间:2022/08/22 点击数:一、前言
T细胞疗法包括CAR-T和TCR-T等已成为一种高效的新型治疗肿瘤尤其是血液瘤的方法。以往细胞治疗的治疗剂量是根据呈递相关表面抗原的细胞总数来计算的,希望这些细胞的部分群体能够在移植到病人体内表现出持久的效应反应。最近的研究表明呈现中央记忆表型的T细胞在多种疾病模型中会提高效应表型的疗效[文献1]。
如图1所示,TCM是中央记忆型T细胞(Central Memory T cell)的简称,是初始T细胞(Naive T Cell)经过抗原激活后,产生的具有长期记忆性的,并能够归巢到淋巴结接受抗原再刺激的T细胞。被激活的TCM细胞,在抗原的再次刺激之下,可继续产生大量的携带同种抗原的克隆化的效应记忆型T细胞。因此TCM细胞因其归巢性、记忆性、持久性以及扩增性等抗肿瘤的特点,相对于以效应T细胞为主成分的免疫细胞治疗生物制品具备一定的预防/抗肿瘤和治疗肿瘤双重作用的优势。
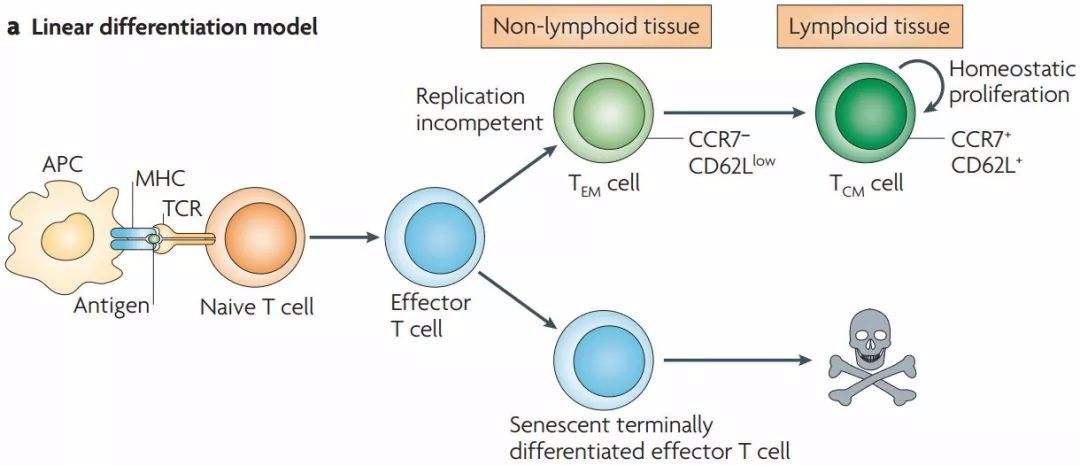
图1 中央记忆T细胞TCM的分化由来
免疫治疗用细胞体外培养体系尤其是培养基补充剂的可持续性稳定供应是诸多生物医药企业密切关注的问题之一。细胞治疗行业的迅速发展给传统的细胞培养物料的传统供应链带来了压力,胎牛血清作为一种动物衍生试剂在监管方面存在重大问题,因此研究人员在很大程度上依赖于人类 AB血清作为一种特殊的蛋白质、激素和细胞因子混合的补充来源,以此促进T细胞制造过程中的生长。然而人AB血清除了本身原材料对于供体选择的限制性问题,在能否保持细胞特定表型或重要特性的情况下能否比FBS更能促进细胞增殖的作用是有争议的[文献2]。
人血小板裂解液Human Platelet Lysate (hPL)是作为胎牛血清、人AB血清的替代性的培养基补充剂,hPL是将人的血小板进一步裂解后所获得的液体成分,其中含有多种生物活性因子(如图2)。
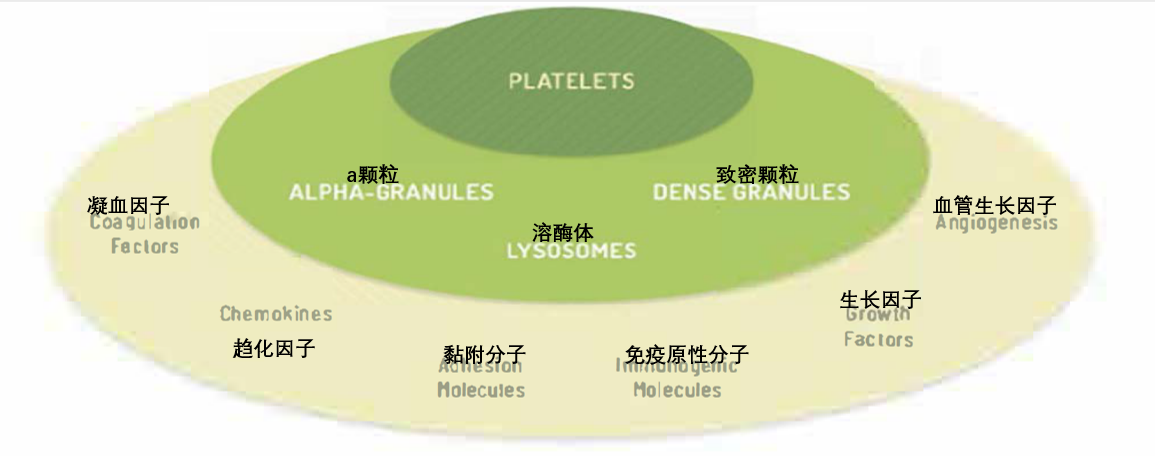
图2 血小板裂解液hPL组成成分
日立先进治疗方案公司(HCATS)和美国Sexton生物技术公司合作将人血小板裂解液nLiven PR与人AB血清(ABS)作为两种免疫细胞治疗用细胞培养基补充剂在对T细胞记忆表型和细胞扩增性能影响差异进行了小规模评估,以期研究如何帮助细胞治疗的生物医药企业提高细胞治疗用的细胞质量和增加细胞稳定供应。
二、T细胞培养扩增以及TCM表型实验
1、hPL与ABS对细胞扩增群体效果比较
从两个供体获得外周血单个核细胞(PBMCs),用CD3/CD28 T细胞激活剂后在静态培养瓶条件下培养14天。总的来说,在培养第8天时总PBMCs细胞数扩增没有明显变化,然而在第10天使用nLiven PR的培养组在两个供体中都显示出明显高于ABS的扩增效果(图3)。并且对于第8天细胞样本进行的FACS分析,其中nLiven PR组中CD3+细胞亚群比例增加到98.2% ± 0.24%(供体1) 和 97.6± 0.26%(供体2),而ABS组CD3+细胞亚群比例分别为94.8%±0.63%和91.9%±1.47%。因此可初步大致判断nLiven组相对ABS组的PBMCs总扩增群体增加的原因是由于T细胞亚群为主扩增的促进。
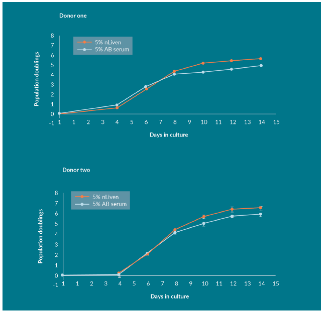
图3:两名捐赠者的 PBMCs 在以 ABS 和 hPL 作为培养补充剂的扩增对比
培养10天后均实现了统计学上显著的扩张
2、hPL与ABS对细胞扩增时TCM细胞亚群影响的比较
在前言中,我们已知TCM的定量化的监测为临床规范化治疗提供参考指标,通过细胞制剂中最终TCM亚群而不是总T细胞产量来评估培养效果提供更现实的治疗相关性参考,因此可以说良好TCM表型的T细胞群体也是评估细胞治疗制剂的产量有效且重要的参考方面。
一般而言TCM细胞亚群的百分比通常与细胞群体翻倍的次数呈负相关(如图4中的ABS培养组),然而当在静态培养瓶中用nLiven PR培养时,与ABS组相比虽然实验中细胞总产量相似但是该TCM亚群细胞在统计上有显著增加(见图4),由此推断nLiven PR条件下生产的高质量、有效的TCM细胞数量更多。这也再次验证了实验1中得出的结论:无论不同的供体PBMCs中TCM的起始浓度百分比是多少,14天培养期结束时有大约30%的T细胞群体为TCM(起始细胞为PBMCs) ,但同样利用ABS培养的 PBMCs扩增的同时则会导致TCM群体显著减少。
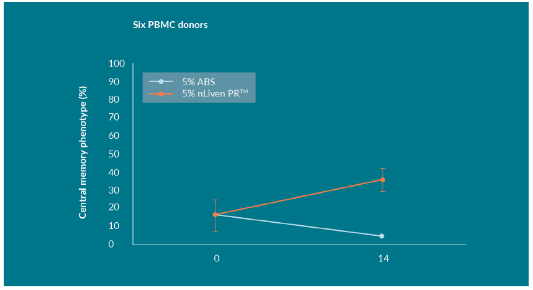
图4:来自6个独立供体实验的数据在静态培养瓶中扩增显示
nLiven PR在培养14天后持续增加PBMCs中总的中央记忆T细胞比例
下图5种展示的是起始细胞选用来自三个供体的CD3+阳性的细胞,在结束培养期时约50%的T细胞亚群为TCM。nLiven组与ABS组相比,两名供体的PBMCs细胞培养后TCM细胞亚群有统计学意义的显著增加。
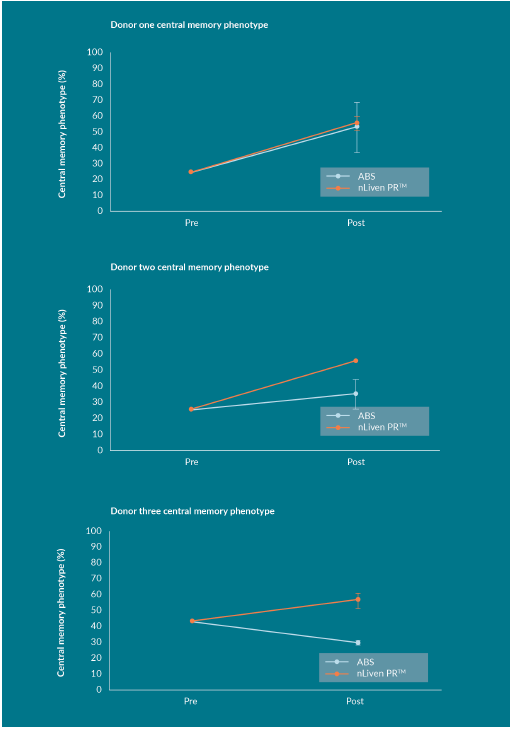
图5:三个供体的CD3+阳性的细胞用hPL和AB血清扩增后TCM的比例
用nLiven PR培养的T细胞在体外扩增实验中,其TCM细胞亚群的增加结果趋势是明确且保持一致的,这与添加AB血清培养获得的T细胞包括增效果随之而来的TCM亚群比例降低的这种现象即原代人T细胞扩增的驱动向效应表型分化的预期相反,这表明nLiven PR的作为T细胞培养基补充剂的加入有选择性地促进了在整个体外培养过程中TCM表型的维持。
3、hPL与ABS对T细胞治疗起始材料差异性影响的比较
紧接着研究人员在放大的搅拌培养系统中评估使用nLiven替代ABS作为培养补充剂的持续影响,主要操作是:对于来自三个供体的CD3+起始细胞亚群,用Dynabeads-Activator CD3/CD28 激活处理后,在搅拌式生物反应器中培养11天。发现nLiven PR和ABS两组的所有三个供体的平均细胞群的翻倍分别为6.1±0.58和6.0±1.37 (图6)。因此该实验中nLiven和ABS两组总T细胞群体扩增没有统计学上的显著变化。然而当关注到这三组间供体来源起始细胞群体CD3+之间的差异性,nLiven PR组的变异系数为10%,而ABS组为23%,由此表明nLiven PR组的供体间变异显著降低,后面的实验也在这两组不同供体间的对比实验发现nLiven血小板裂解液作为培养基补充可能会缓解因血小板捐赠供体之间差异性带来的整体治疗的差异性影响,降低起始材料的可变性,帮助开发者产生更好的特征治疗。
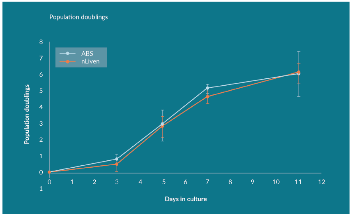
图6:3组供体来源的T细胞扩增在ABS和hPL两种组影响区别不大
但nLiven PR组的供体对供体变异显著较低
如何降低批次之间的差异是开发细胞治疗制品一个主要考虑因素,作为人类血小板的裂解物nLiven比富集的人AB血清在生产制备工艺过程中涉及生物化学物质的更为均匀的混合。这种差异可能是带来细胞治疗用细胞培养产生更为一致反应的原因之一。
三、结语
本次研究多个供实验中,nLiven PR的培养组中TCM表型得到促进即在PBMCs扩增的TCM细胞亚群显著增加。而对于细胞制品转化为临床时关注的捐赠供体的一致性影响方面:与ABS相比,当nLiven PR补充培养基进行与商业相关的细胞培养扩增实验时,不同供体间获得的总细胞产量或中央记忆表型TCM的变异水平较低。从细胞制剂中所用治疗用细胞质量的属性,而不是细胞数量的体积来评估产量方面,我们可以得出:nLiven 将PR应用到T细胞体外细胞制品的制造过程中可以获得高质量的治疗用T细胞。
此外美国贝勒医学院由 Norihiro Watanabe利用胎牛血清(FBS)、人AB血清(ABS)和人血小板裂解液nLiven作为培养基补充剂对T细胞记忆表型和治疗疗效的影响进行了小规模评估,最终结果显示:对比ABS和FBS,在nLiven中培养组实验中,表现出中央记忆表型的T细胞和总存活率在统计上显著增加(图7)[文献3]。
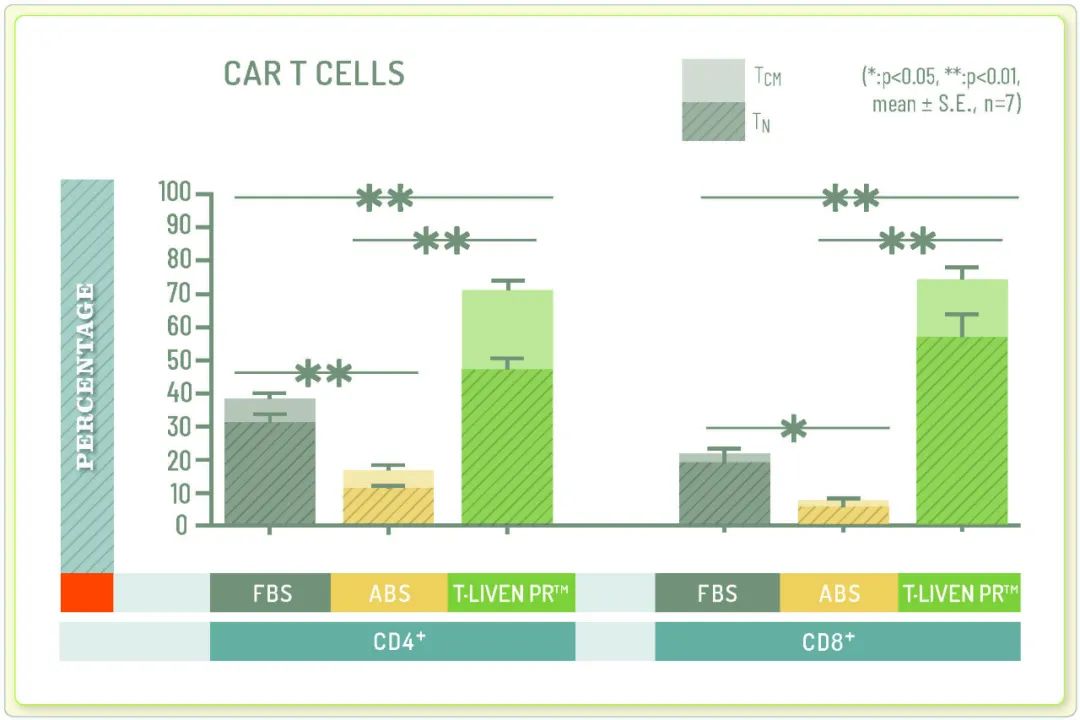
图7:相对于FBS和ABS,Sexton血小板裂解液T-Liven的扩增效率更高,更有助于T细胞维持较低的分化水平状态
美国Sexton公司无动物源无需添加肝素的人血小板裂解液,既提供经典的Stemulate满足干细胞治疗用户科研和临床以及GMP生产需求,又针对免疫细胞治疗提供病原体去除(Pathogen Reduced,PR)工艺的临床级nLiven和袋装封闭系统T-Liven血小板裂解液产品。满足质量和监管要求且已在FDA已经备案药物主文件,是全球临床干细胞和免疫治疗应用中用作高性能FBS/ABS替代品。
封闭袋装系统包装形式的TLiven产品(经T细胞生长验证实验)
美国Sexton品牌 PR工艺
四、参考文献
1.Klebanoff CA, Gattinoni L, Torabi-Parizi P et al. Central memory self/tumor-reac-tive CD8+ T cells confer superior antitumor immunity compared with effector memory T cells. PNAS 2005; 102 (27): 9571–6.
2.Manufacturing of primed mesenchymal stromal cells for therapy. Nature Biomedical Engineering,2019. 3(2): 90-104.
3.Torres Chavez A, McKenna MK, Canes¬trari E et al. Expanding CAR T cells in human platelet lysate renders T cells with in vivo longevity. J. ImmunoTher. Cancer 2019; 7: 330.