发布时间:2023/10/11 点击数:
发布时间:2023/10/11 点击数:将人类淋巴母细胞(TK6细胞)集成到肝脏芯片中用于基因毒性测试:顺应潮流,减少动物实验

本文概况
来自国际知名的药物发现和临床前服务实验室--Charles River的研究团队,将英国CN-Bio的肝脏芯片(Liver-on-Chip,LOC)技术,应用于遗传毒性测试,初次产生了更有预测性的人体结果,潜在地有助于弥补体外和体内研究之间的差距。
前言
目前的体外临床前遗传毒性测试体系包括在单个细胞和细菌中使用代谢活化系统"Induced rat S9 mix",来确定药物代谢和遗传毒性。"Induced rat S9 mix"试剂主要由Sprague Dawley(SD)大鼠肝脏的S9部分构成,富含药物代谢酶,包括P-450等。
在临床前研究中,大量药物开发失败是由于意外的毒性效应,通常与肝脏生物转化有关(种间差异性)。来自Charles River的研究团队将CN-Bio的肝脏芯片(Liver-on-Chip,LOC)技术,应用于遗传毒性测试产生了更有预测性的人体结果,潜在地有助于弥补体外和体内研究之间的差距(图1)。

图1 - 肝脏芯片 (Liver-on-Chip,LOC) 可能有助于弥补体内和体外研究之间的差距。
研究目标
本研究的目标是重建具有人类代谢功能的肝脏芯片(Liver-on-Chip,LOC)的 3D 器官微环境,采用原代人肝细胞(PHH)或HepaRG细胞构建,与人类淋巴母细胞(TK6细胞)进行共培养,从而用于遗传毒性评估。
材料与方法
如下图2:
(A)采用与遗传毒性测试中体内试验相同的时间表进行处理,(B)用于培养共培养系统的板,(C)微生理系统(Microphysiological System,MPS)
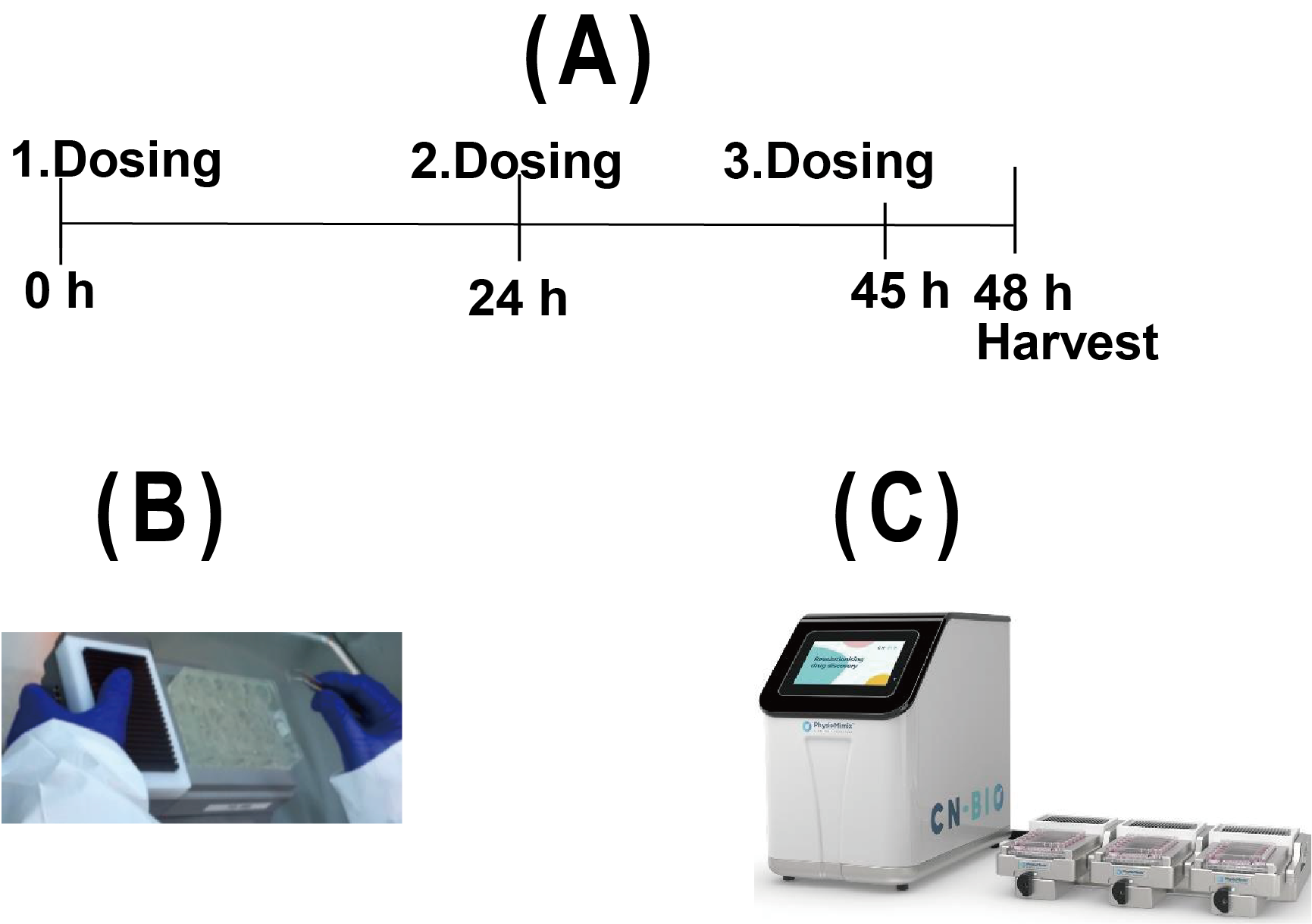
图2
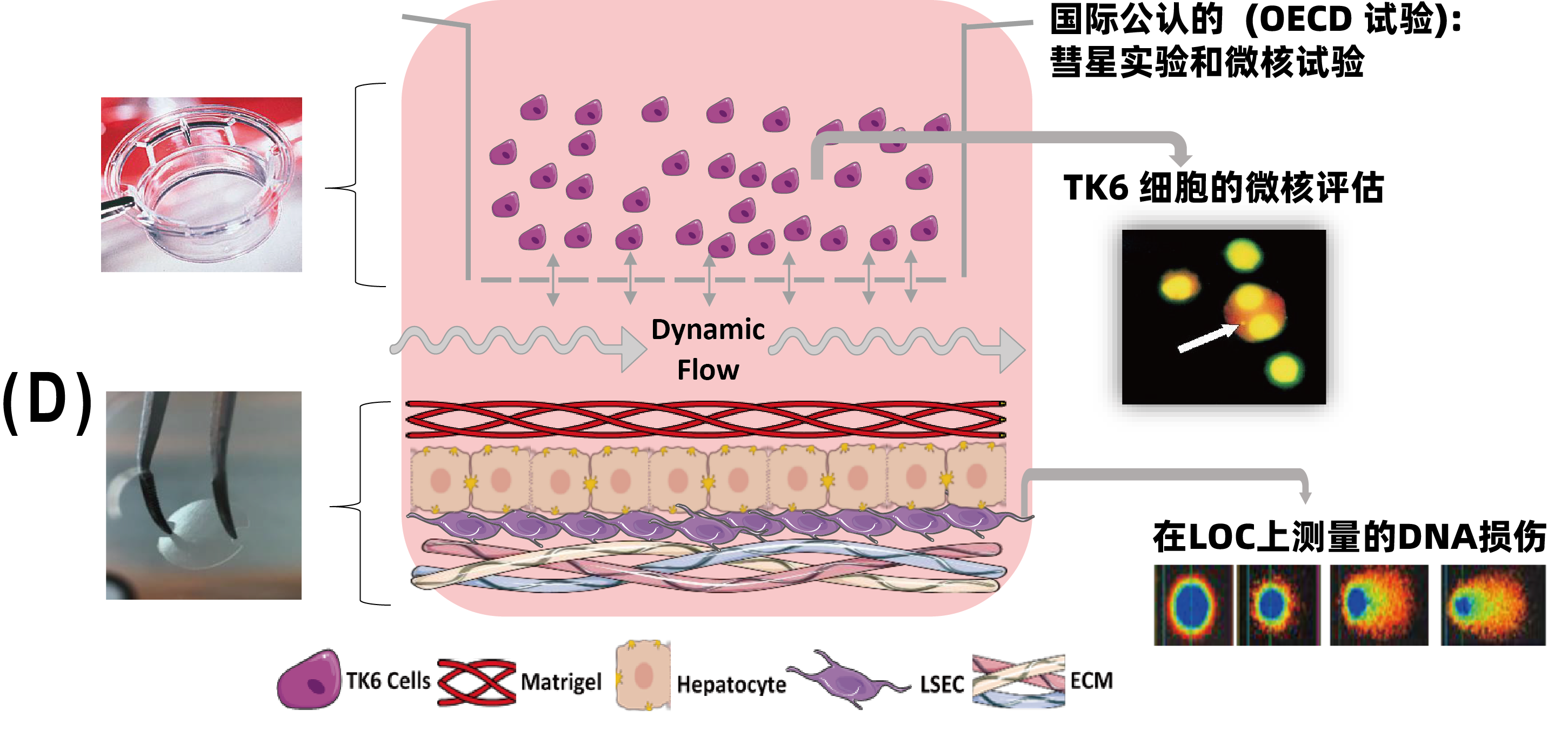
(D)肝脏芯片(Liver-on-chip,LOC)与TK6细胞共培养的示意图,并说明如何将每种测定方法适应于该系统。该LOC由原代人肝细胞(PHH-LOC)或HepaRG细胞(HepaRG-LOC)以及TK6细胞组成。该系统允许两个隔室之间的通信,并进行多种终点分析,例如肝细胞中的彗星试验(% tail DNA intensity)和TK6细胞中的微核试验(使用MicroFlow试剂盒(Litron)进行流式细胞术)。两个LOC(包括细胞外基质、内皮细胞、PHH或HepaRG和Matrigel)均在CN-Bio的器官芯片系统技术下维持,TK6细胞在Transwell上进行培养。两个隔室分别在0、24和45小时时,使用阴性对照、直接诱变剂甲烷磺酸酯(5μg/mL的MMS)或间接诱变剂苯并[a]芘(10μg/mL的BaP)和环磷酰胺(50μg/mL的CP)进行处理,阳性对照使用变异诱导剂乙基甲磺酸酯(EMS)。进行了三次独立实验,并收集了肝细胞和TK6细胞。
结果与讨论
1、在共培养系统中的存活情况
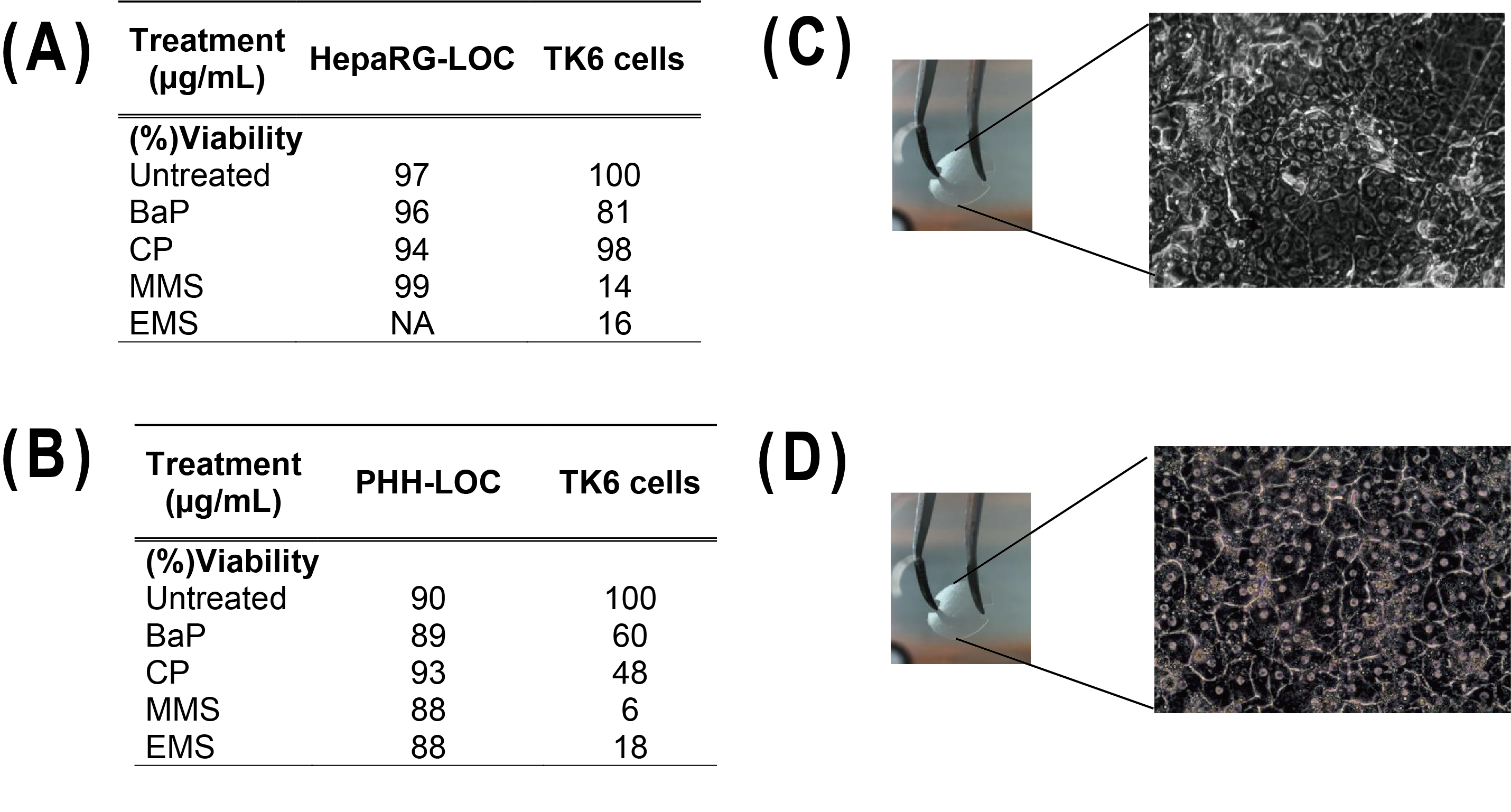
图3:从LOC获得的单细胞悬液的存活情况进行了评估(台盼蓝染色法),并对TK6细胞进行了流式细胞分析。从与TK6细胞共培养的HepaRG构建的LOC(A)和与TK6细胞共培养的PHH构建的LOC(B)获得的%存活率结果。NA=不适用。在微流控流动条件下培养了9天后的(C)HepaRG-LOC和(D)PHH-LOC的显微镜图像。
2、HepaRG细胞构建的肝脏芯片成功地证明了,使用CP获得的数据与使用相同试验描述的体内研究直接相关:在肝脏中影响不大(%Tail DNA),但在淋巴(TK6)细胞中表现为正面响应(% MN 增加)。这些发现在HepaRG的2D模型或3D球体模型中并未出现。
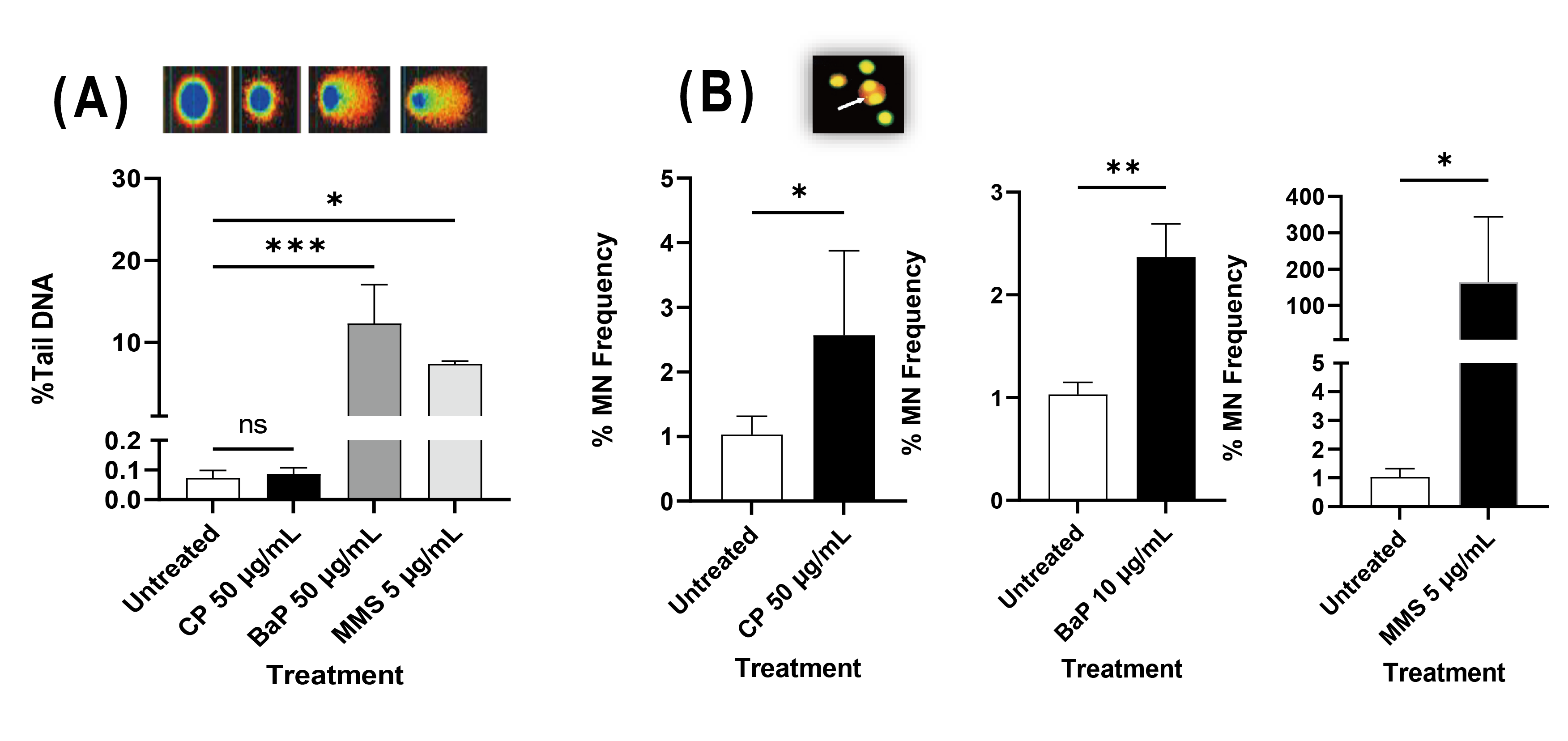
图4:来自至少三次独立实验的结果。
(A)使用HepaRG的HepaRG-LOC中HepaRG的彗星试验结果。DNA损伤水平(% Tail DNA)。统计分析采用一元方差分析(one-way ANOVA)后进行Dunnet's多重比较检验:*p<0.05,**p<0.01,***p<0.001,****p<0.0001,ns=不显著。
(B)使用HepaRG的HepaRG-LOC的TK6细胞微核试验结果。微核频率(% MN frequency)。统计分析采用t检验进行,其中*p<0.05,**p≤0.005,****p<0.001。
3、使用原代人类肝细胞(PHH)构建的肝脏芯片,TK6的结果表明,PHH-LOC更有效地代谢了测试的间接诱变剂(CP和BaP),尽管在初级人类肝细胞中某些活性较低或较高,这很可能反映了供体之间的差异。
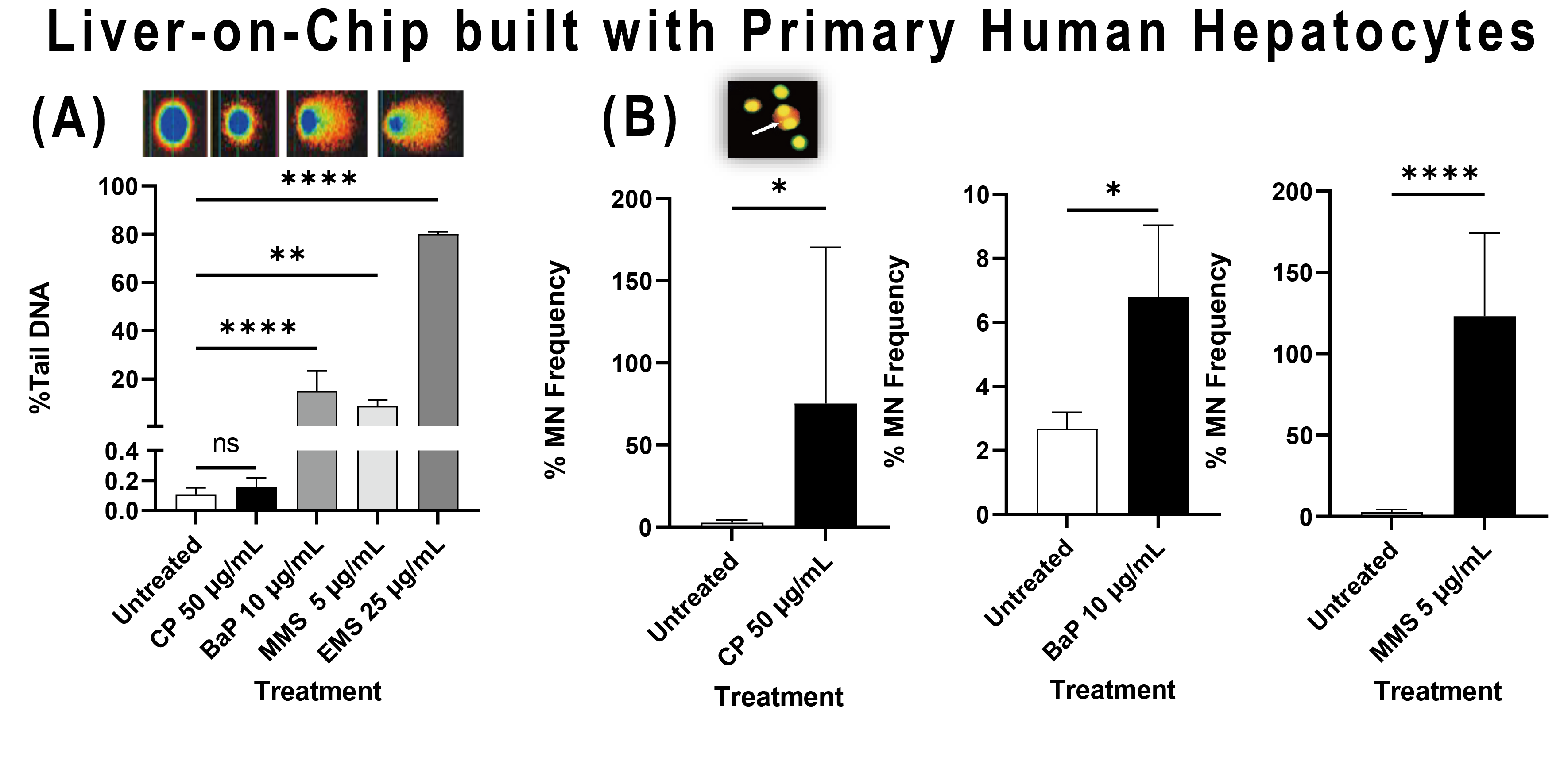
图5:
(A)这些结果来自至少三次独立的实验。在使用PHH的PHH with LOC中进行的彗星试验结果显示,通过一元方差分析(ANOVA)和随后的Dunnet多重比较检验进行统计分析:* p< 0.05 , ** p< 0.01, *** p < 0.001, **** p < 0.0001,ns= 非显著。
(B)在使用PHH构建的肝脏芯片的TK6细胞中进行的微核(MN)试验结果显示,微核水平(% MN频率)。统计分析采用t检验,其中 * p< 0.05 , ** p ≤ 0.005, **** p < 0.001。
结论
1.本研究初次报道了微体系生理学(MPS)在遗传毒理学测试中的应用。
2.两种生理微环境系统均表现出代谢特性,并具有在一个系统内处理两种遗传毒性不良结果的能力,即诱发染色体损伤或有丝分裂装置损伤(微核试验)和DNA链断裂(彗星试验)。
3.本研究显示,生理微环境系统可能是一种有前景的工具,可以更好地弥补体内外研究之间的差距,因此在遗传毒理学领域应进一步探讨。
推荐阅读
【点击文字阅读】CN-Bio器官芯片应用 ——非酒精性脂肪肝炎(NASH)
【点击文字阅读】多器官芯片系统应用(一) ——药物的药代动力学
参考文献
(1) Mandon, M., Huet, S., Dubreil, E.,Fessard, V., Le Hegarat, L. Three-dimensional HepaRG spheroids as liver model to study human genotoxicity in vitro with the single cell gel electrophoresis assay. Scientific Reports. 2019; 10548.
(2) Recio, L., Hobbs, C., Caspary, W., Witt, K.L. Dosed-Response Assesment of four genotoxic chemicals in a combined mouse and rat micronucleus and comet assay protocol. J Toxicol Sci. 2010; 35 (2): 149–162.
(3) G. (2013, December 20). File:vector diagram of laboratory mouse (black and white).svg. Retrieved February 16, 2021, from https://commons.wikimedia.org/wiki/File:Vector_diagram_of_laboratory_mouse_(black_and_white).svg