发布时间:2023/12/07 点击数:
发布时间:2023/12/07 点击数:声明:上海曼博生物医药科技有限公司是英国CN-Bio官方授权的中国代理商,对器官芯片感兴趣的用户欢迎咨询上海曼博生物,本文由曼博生物翻译编辑。
一、FDA 现代化法案 2.0 是什么?它的含义是什么?
美国食品和药物管理局 (FDA) 是负责批准新药在美国 (US) 境内使用的联邦机构。2022 年 9 月29 日,美国参议院一致通过了 S.5002 号法案,即“FDA 现代化法案 2.0”。2022年12月23日,美国众议院批准。随后,拜登总统将其签署成为法律。在这一具有里程碑意义的措施中,可追溯至 1938 年的《联邦食品、药品和化妆品法案》现在将进行更新,以反映现代科学的进步。但为什么这有这么大的事呢?
起初的法案规定,所有药物在人体临床试验之前都必须在动物身上进行测试。这项法律是为了应对磺胺酊剂的销售而通过的,这种有毒药物已导致 100 多人死亡!这在 20 世纪 30 年代是完全有道理的,当时动物试验是临床试验前测试药物安全性的非人类方法,但自那以后,科学技术已经取得了长足的进步。事实上,到目前为止,规定必须在动物身上进行药物测试的联邦命令现已被取消。在适当的情况下,可以采用新方法方法(也称为新替代方法或 NAM)来确定药物的安全性和有效性,以代替动物试验。
在 FDA 现代化法案 2.0 题为“动物测试替代方案”的第 3209 条中,该法案修改了 FDA 要求对药物和生物仿制药进行动物测试的监管指南。该法案对《联邦食品、药品和化妆品法》(FFDCA) 进行了修订:
· 用“非临床试验”一词代替当前的“临床前试验”(包括动物试验)
· 将术语“动物”替换为“非临床测试”
· 添加定义“非临床测试”的新部分,包括与人类相关的测试方法,例如基于细胞的测定、微生理系统(例如器官芯片)或生物打印或计算机模型。
二、是什么推动了政策变化?
道德考虑显然是一个重要的驱动因素,因为没有人希望动物被不必要地使用,更有效地将新药推向市场的愿望是另一个驱动因素。90% 的药物在临床试验中仍然失败,因为它们缺乏疗效或存在安全问题。根本原因是临床前模型无法预测人类的这些反应。
此外,发现管道不再仅仅充满小分子药物。新药物模式约占产品线的 20%,其针对人类的作用模式意味着动物模型不太适合他们的测试。认识到这一需求并支持 FDA 现代化法案 2.0 的通过,药物发现公司和 FDA 一直在与像我们这样的公司合作,推动 NAM 领域的科学和创新。微生理系统(MPS),也称为芯片器官(OOC)特别令人感兴趣,因为它们允许研究人员重新创建一个准确代表人体并生成临床可翻译数据的测试环境。
MPS 技术使用户能够使用原代人体细胞的相关组合在实验室中重建三维 (3D) 器官和组织。液体在组织中循环以提供营养并模拟血液流动。其结果是实验室培育的模拟物能够以与人类相同的方式发挥作用并对药物做出反应。此外,它们可以连接在一起来模拟药物吸收和代谢等过程,或了解器官之间的相互作用,例如炎症,炎症会导致疾病并引起意想不到的毒性。通过这样做,他们为测试具有人类特定作用模式的药物提供了动物的替代方案。
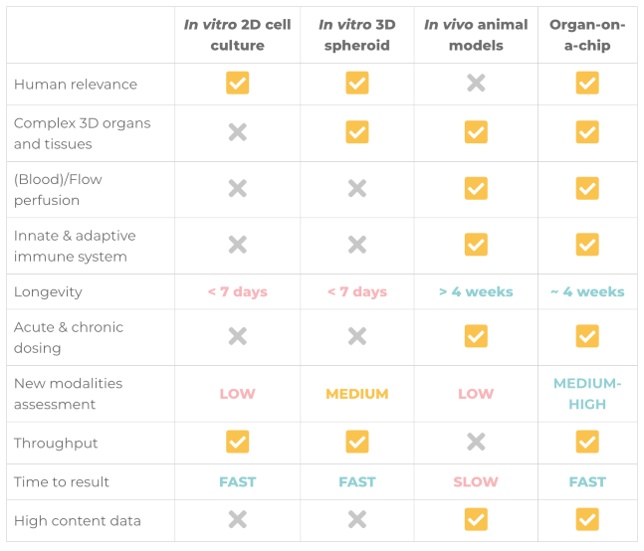
由于 MPS 的潜力,修订后的 FDA 现代化法案第 3209 节特别引用了 MPS,而且这种与人体相关的测试方法已经得到 FDA 本身的认可。在最近经过同行评议的第一份出版物中1,FDA 证明了我们的 PhysioMimix 肝脏芯片(或肝脏微生理系统)在药物代谢和毒性应用方面比传统方法具有改进的性能。在过去的 5 年里,我们一直保持着强有力的合作,并扩展到评估多个临床前应用的其他器官模型的性能。
三、这对药物开发商意味着什么?
显然迫切需要将更多可人类翻译的体外模型纳入临床前工作流程。随着 FDA 现代化法案 2.0 的通过,美国的药物开发商现在有了更多的选择,减少了对动物模型的依赖!他们可以在药物发现的早期自由选择更合适的应用方法,而不是被迫走动物路线。改变不会在一夜之间发生。技术需要得到验证,需要赢得信任,旧习惯很难改掉,SOP 需要很长时间才能改变……但现在:
· MPS 可在药物发现之初使用,以验证模型中的目标,从而更准确地代表人类疾病
· MPS 可在动物研究之前使用,以测试大量条件/完善条件/更大限度地减少所需动物数量
· MPS 可与动物一起使用来确认或查询结果,降低因种间差异而出现不可预见问题的风险
通过生成人类可翻译的数据,MPS 提供了一个机会,可以尽早重新设计可能存在缺陷的药物,以更大限度地提高它们在进入临床后的成功机会。
在某些情况下,NAM 提供了一种动物替代品,更大限度地减少了对人类的可翻译性较差的动物的不必要使用。
通过使研究人员能够将技术更先进的工具纳入他们的工具箱,将改善向市场提供急需的治疗药物的成本/时间。时间会揭晓真正的结果,然而,独立研究估计,将 OOC 完全整合到制药工作流程中可以节省高达 26% 的研发成本2。
四、这对于 NAM 提供商(包括我们 CN Bio)意味着什么?
这意味着聚光灯已经亮了。多年的努力确保我们已做好迎接挑战的准备,这是一个令人兴奋的地方。在幕后,像我们这样的公司十多年来一直在开发这项技术、先进的单器官和多器官 MPS 及其适用性(在疾病建模、毒性测试和 ADME 领域)。通过与学术界、药物发现公司、联盟(例如IQ 联盟)和各种监管机构的合作,我们共同收集了大量证据,以证明这些与人类相关的模型能够提供更好地预测人类结果的数据。我们的技术已准备好沿着修订后的 FDA 现代化法案中提出的前进道路发展。
我们还与北美 3R 协作组织(NA3RsC) 和英国无动物研究中心(AFRUK)等组织合作,提高人们对 MPS 技术作为动物替代品的认识。在提到英国的同时,这让我想到了另一个重要的观点。值得注意的是,尽管美国是第一个迈出这一步的监管机构,但其他地区也在开展重要工作来推动变革。早在 2014 年,英国就宣布了减少科学研究中动物测试使用的计划,旨在尽可能用“科学上有效的替代方案”取代这些测试。最近在 2021 年,欧洲议会投票支持逐步取消研究中动物测试的计划。去年,专注于帮助推动新技术采用的欧洲标准化委员会CEN成立了 OOC 焦点小组和欧洲器官芯片协会(EUROoCS)等非营利组织自 2018 年以来,我们一直在扩大其网络,以分享和推进该领域的知识,以改善所有人的健康。
对于我们个人来说,我们的开发团队非常忙碌,因为我们不断在这个领域进行完善、完善、验证和创新,以支持 MPS 使用的需求。我们的重点是解决目前尚未得到满足的临床前药物发现领域。这包括促进治疗方法的发现,以解决未满足的疾病(例如非酒精性脂肪性肝炎),模拟人类肺部、我们的免疫系统、我们的肠道微生物群,克服开发具有人类特异性作用模式和目标的药物的挑战……开发也可用于系统测试的人体芯片。然而,我们的研发时间的很大一部分都集中在促进 OOC 应用于临床前工作流程中。归根结底,如果成本昂贵得令人望而却步,世界各地的实验室无法重新创建它们,并且无法提供有意义、稳健和可靠的模型,那么拥有与人类相关的模型就没有意义数据。
因此,尽管 FDA 现代化法案的通过代表了一个重要的里程碑,但实际上,这代表了一本尚未撰写的非常令人兴奋的书的第一章。然而,既然地球上zui大的监管机构已经迈出了第一步,我们祈祷其他人也会效仿。如果情况确实如此,并且 NAMS 兑现了他们的承诺,那么我们都是赢家——人类、行业和我们毛茸茸的朋友。但就目前而言,我们期待着欢迎新客户——大门已经为他们敞开——并分享他们不断发展的成功故事。
参考文献
1.Rubiano et al. 2020
2.Franzen et al. 2019