
 发布时间:2025/07/24 点击数:715
发布时间:2025/07/24 点击数:715 摘要:Axol及NETRI神经芯片助力NMJ模型升级,推动ALS药物发现
人体iPSC神经肌肉接头建模旨在建立一个支持骨骼肌细胞和运动神经元在同一环境中生长的体外系统。利用iPSC技术,研究人员从ALS患者和非ALS患者的iPSC中分化出多种相关细胞类型。细胞在单层培养中培养并进行表征,之后也在2D微流控装置中研究,在这里观察到它们能形成神经肌肉接头(NMJ),并展示出可量化的ALS相关表型差异。这表明该系统在ALS研究和药物发现中具有潜在应用价值。
一、iPSCs细胞株信息--来自渐冻症供者和未受影响供者
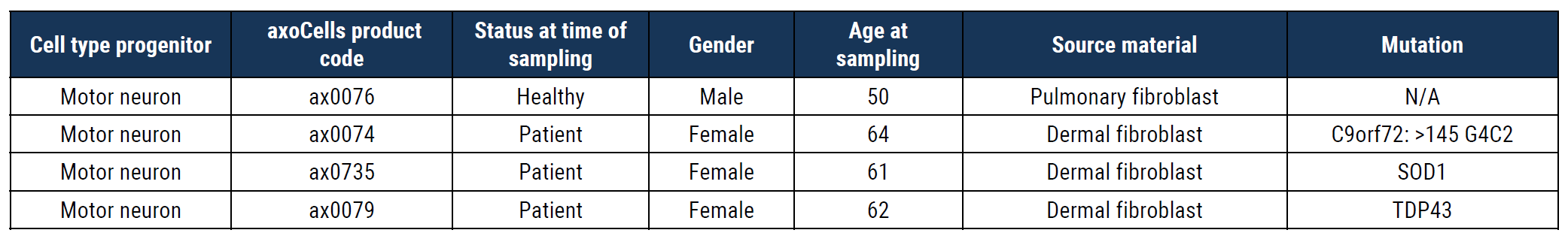
二、人iPSC衍生的运动神经元表征
根据Axol公司独特的方法,从ALS患者和健康供体的iPSC中生成了运动神经元前体细胞。
• 通过免疫组化(ICC)检测这些细胞,分析它们是否表达运动神经元相关的标志物,检测时间是在解冻和成熟后的第10天。
• 使用莱卡成像系统和FIJI软件对细胞标志物的信号进行量化,结果如下:Tuj-1 = 100%,HB9 ≥ 80%,Chat ≥ 90%,Isl-1 ≥ 80%。
• 这些细胞还通过多电极阵列(MEA)进一步表征,结果显示它们具有自发和同步的爆发性放电活动。
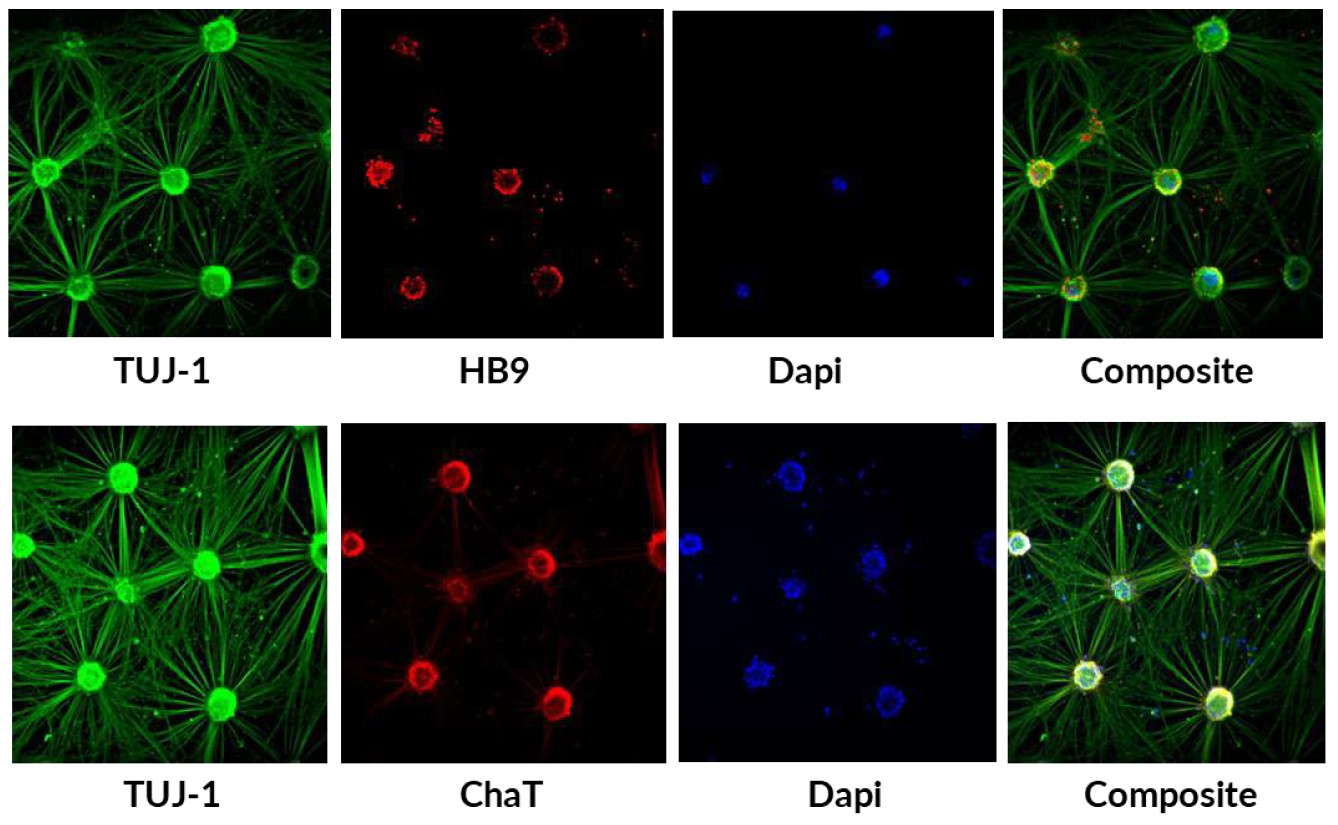
图1.axoCells人诱导多能干细胞衍生的运动神经元的免疫细胞化学染色(未受影响的供体)
三、iPSC衍生的运动神经元中ALS相关功能表型

图2.从解冻后第10天开始,iPSC衍生的运动神经元通过成像和MEA分析,展示了不同的功能和形态表型
四、人iPSC衍生肌管表征
肌管是通过人iPSC生成的肌母细胞前体。
• 第5天,使用免疫组化(ICC)检测骨骼肌细胞的特定标志物,并使用莱卡成像系统和FIJI软件对细胞标志物进行量化。
• Actin ≥ 80%,Titin ≥ 80%,MyoD1 ≤ 10%,Myosin-HC ≥ 50%,Myogenin ≥ 50%,Dystrophin ≥ 80%。
• 肌管是多核的(每个核有4-5个核),并显示出明显的肌节结构,表明其为肌管/骨骼肌形态。
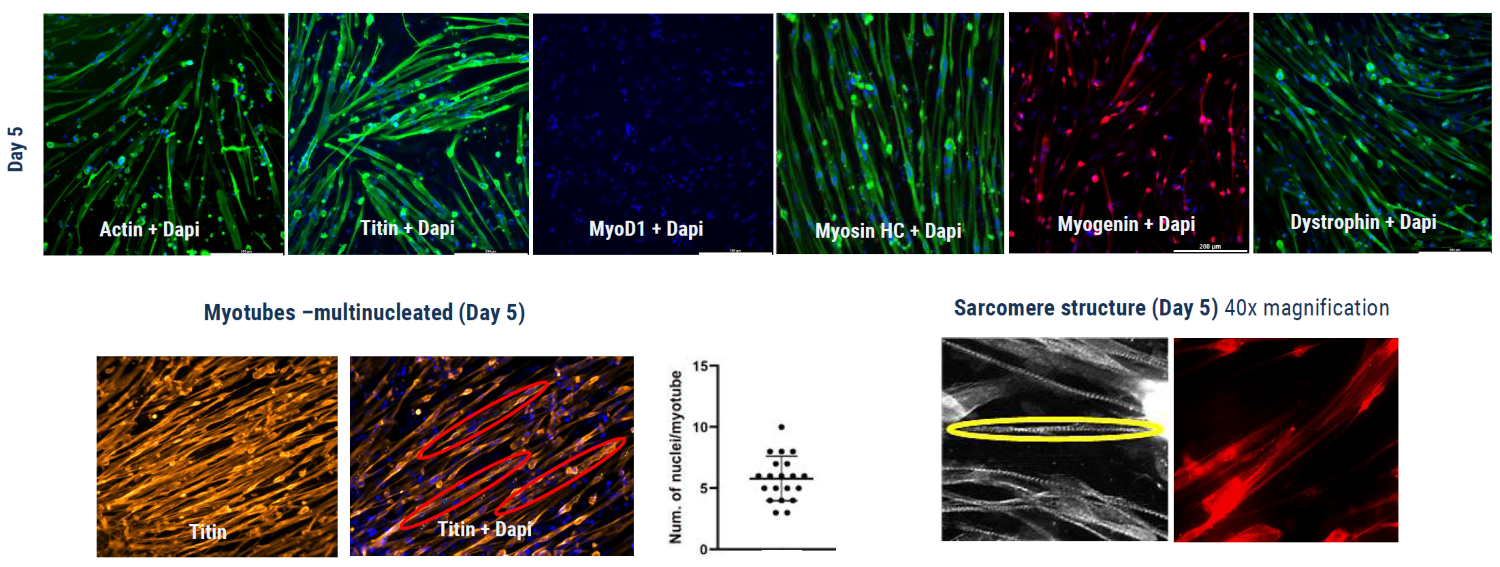
图3.人iPSC衍生的肌管(unaffected donor)
五、在一个与MEA兼容的双腔微流控系统中建模神经肌肉接头(NMJ)
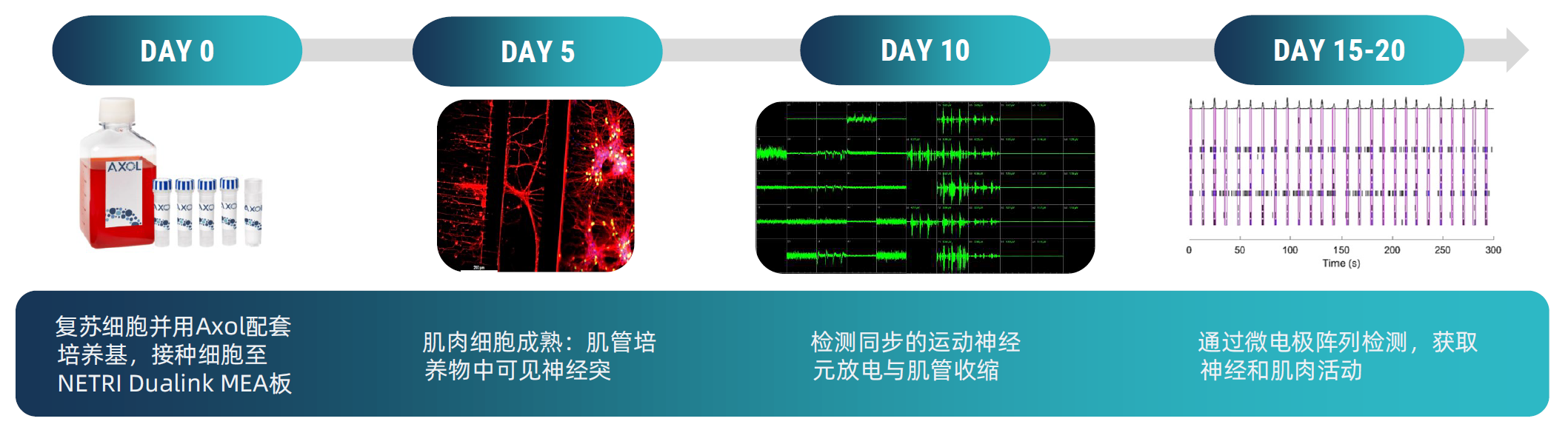
图4.成功在NETRI Dualink双腔微流控系统中建立了iPSC来源的运动神经元和肌管培养体系,并且该系统还能够进行成像和MEA分析。
NETRI的DuaLink chip,专为共培养最多2种细胞类型和流体隔离而设计,如:运动神经元和骨骼肌细胞、皮肤角质形成细胞和感觉神经元。其微通道技术可增降轴突投射,将神经突触与神经元胞体准确区分。Dualink chip 通量较高,一整块板可培养16组样本,并可选配MEA 来记录神经元的电活动。
关于NETRI其他神经芯片类型,可点击文章阅读 曼博代理 | NETRI神经芯片
六、NETRI DuaLink在第15天的共聚焦图像
• 通道1:白色–阿尔法毒蛇毒素(NMJ突触标记/Titin(肌管))
• 通道2:Tuj1(神经突起标记)
• 通道3:ChAt(运动神经元标记)/ Tuj1
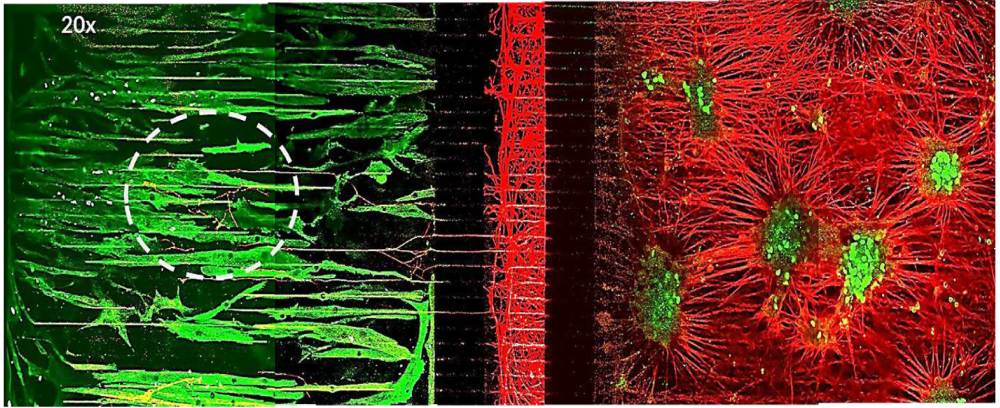
图6.神经突在通道和微通道中穿过,并进入骨骼肌区域(Tuj1 表达呈红色)
七、通过α-毒蛇毒素阳性测定NMJ功能性突触
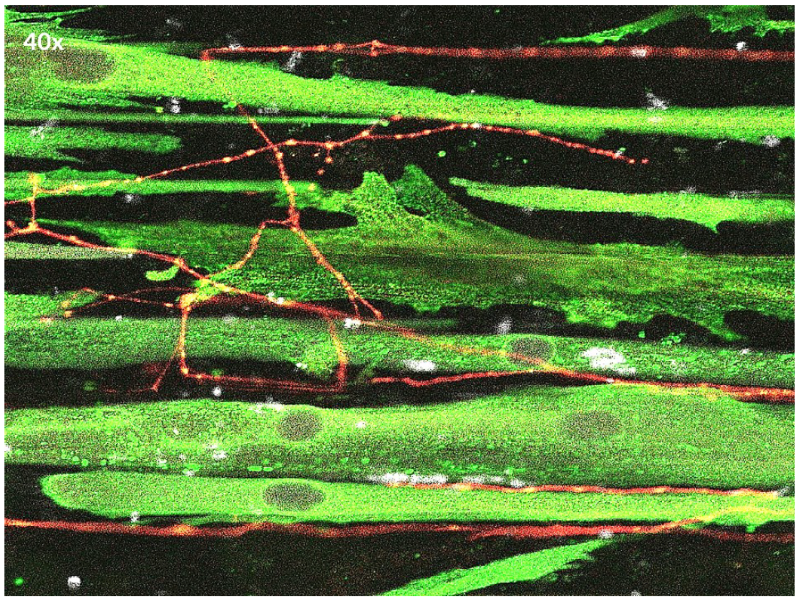
图7.在20倍放大图中,白色小点表示后突触的乙酰胆碱受体α-毒蛇毒素,显示了肌肉和运动神经元的关键功能性神经支配,并且具有功能性的乙酰胆碱神经肌肉接头(NMJ)突触。
八、模型中ALS及其他已知遗传兴趣靶标
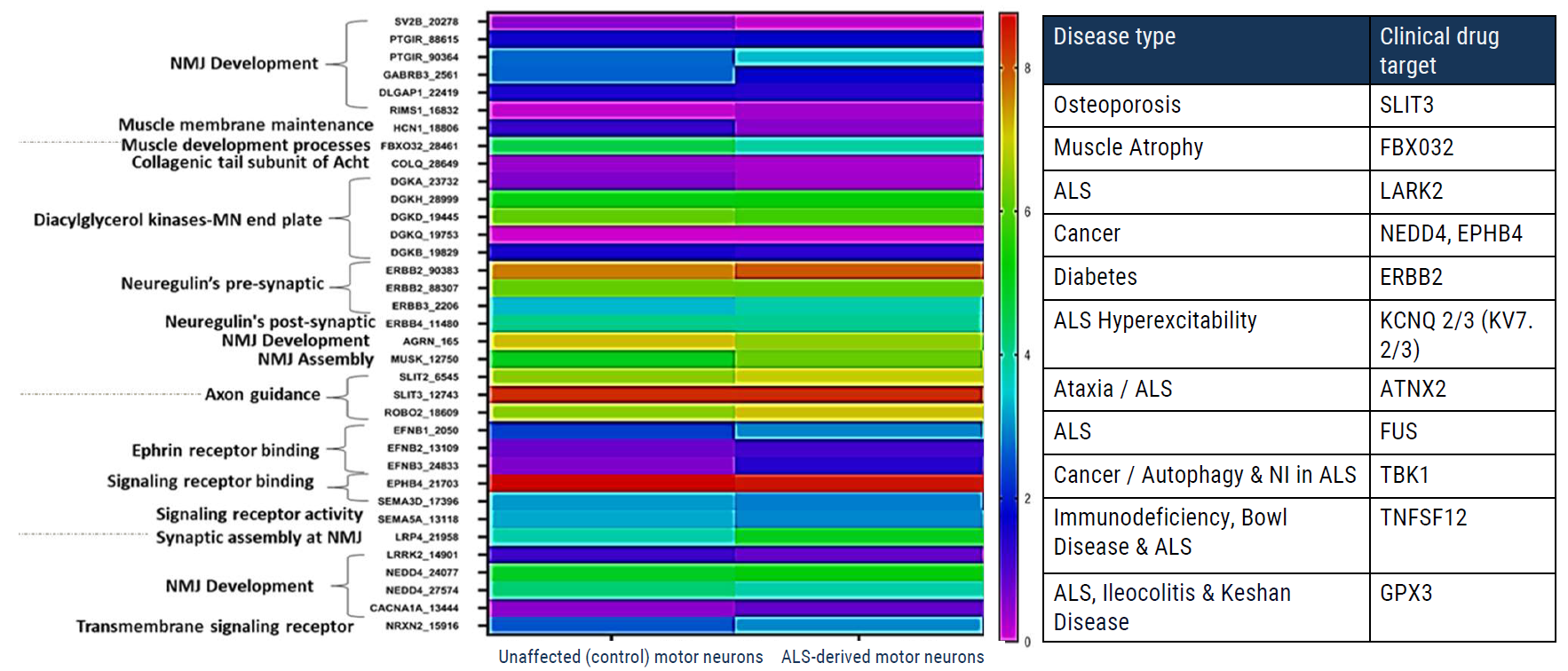
图8.针对多种疾病类型当前临床已知的药物靶标,进行神经肌肉接头及其组件的TempoSeq或RNASeq分析。此图突出了该模型在多种疾病靶标(包括ALS)中的相关性。
九、在ALS神经肌肉接头模型中观察到的超兴奋性
来自神经肌肉接头模型的MEA分析显示,C9orf72运动神经元呈现出可识别的“超兴奋性”表型。
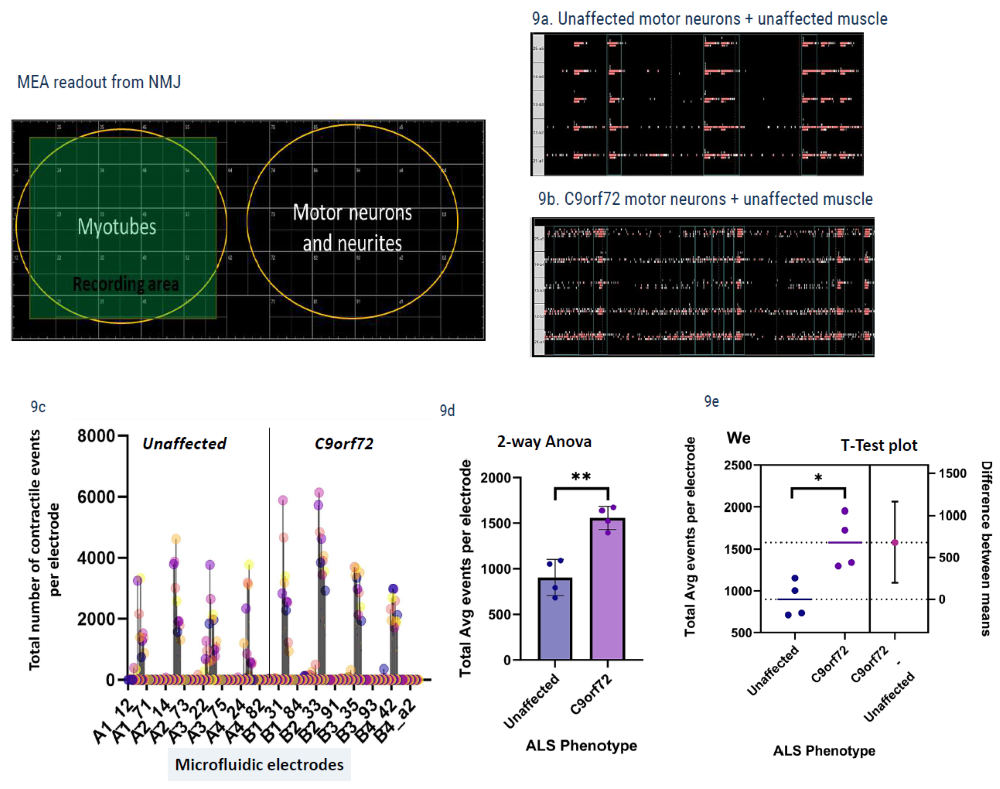
图9右上图 - 概念验证模型,数据误差条表示标准误差(SEM),基于2个芯片上24个生物学独立重复进行肌管引起的收缩性测量。绿色区域(Myotubes):肌管(分化的骨骼肌细胞,模拟肌肉),标注 “Recording area”(电生理记录区);黄色区域(Motor neurons and neurites):运动神经元及其轴突(模拟神经);逻辑:构建神经 - 肌肉共培养模型,研究运动神经元对肌管的激活能力。
图9a-b. Rasta图展示了由运动神经元活动驱动的肌管收缩性。红色波形代表肌管收缩的电活动信号,对比突变型与对照的信号差异(如突变组信号更频繁 / 更强)。C9orf72模型相较于未受影响的模型,观察到活动增加和长时间收缩事件。图9c. 在单个电极水平上评估肌管收缩性,C9orf72突变组(紫色点)的收缩事件远多于对照(Unaffected,彩色点),提示突变运动神经元更易激活肌管。图9d. 通过双向方差分析(2-way Anova)进行统计分析。紫色柱明显高于蓝色柱(**,P<0.01),证明 突变运动神经元对肌管的激活能力更强。图9e. 通过T检验分析,确定未受影响组与C9orf72 ALS群体数据的均值存在差异。
十、结论
• 结合iPSC技术、微流控技术和MEA技术,研究人员能够创建一个功能性的神经肌肉接头(NMJ)模型,这对ALS的研究和药物开发具有重要意义。
• Axol提供的iPSC来源的细胞,在单一培养条件下和双腔微流控环境中都能表现出预期的标记物表达和正常功能。
• 在MEA分析中,研究人员能够量化运动神经元驱动的肌肉收缩,并且在C9orf72模型中观察到了超兴奋性现象,相较于未受影响的供体模型,这种现象更为明显。
• 这类模型不仅适用于ALS的研究,还可以扩展到较广的疾病靶点研究中。
Axol Bioscience是家iPSC技术公司,专注于支持药物发现的advanced模型,特别是神经退行性疾病、神经炎症和心脏毒性领域的研究。

作为iPSC产品和服务提供商, Axol Bioscience致力于开发更具人类相关性的体外模型,推动更安全、更有效的疗法。凭借超过十年的经验,Axol Bioscience为全球前20的生物制药机构和药物研发公司提供高质量的体外模型和定制实验室服务。 Axol Bioscience的技术不仅支持体外疾病模型研究,还提供用于器官芯片和微流控系统的模型量产,从简单的单细胞培养模型到复杂的共培养、三培及3D模型,持续推动iPSC在药物发现中的创新应用。
Axol可为用户提供丰富的细胞类型(部分如下图)
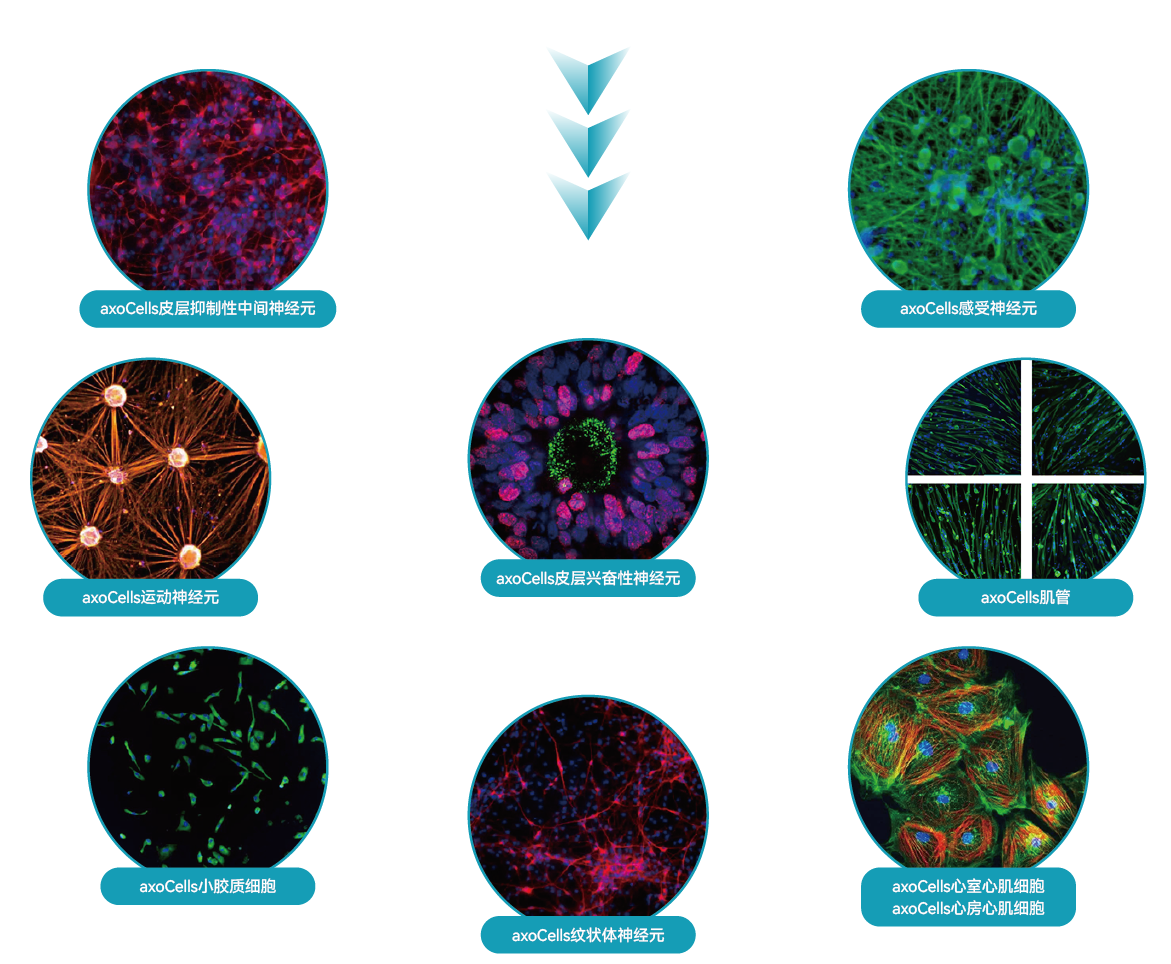

Axol 细胞产品特点及优势
1. 提供丰富的细胞种类:10余种不同类型的细胞
2. 产品在超过1600多篇杂志中被应用和验证
3. 注重功能表现:细胞像神经元一样发挥功能,而不仅仅是外形相似
4. 质量一致性:功能性QC,保障可重复的研究
5. 细胞为共培养而设计:具有更接近生理的特性
6. 快速的成熟时间:使实验更加效率高、经济且可靠
7. 易于使用:配套优化的培养基、试剂、protocol结果
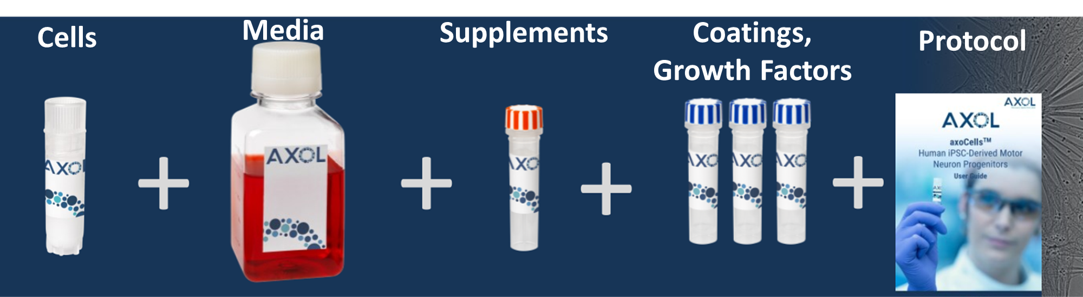
理想结果仅在客户使用上述所有内容时才能获得,方案已尽可能简化和准确。


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 













