
 发布时间:2025/11/27 点击数:587
发布时间:2025/11/27 点击数:587 *注:下文出于保密考虑,已隐去蛋白名称及具体文献引用。
一、引言
转录因子(TFs)是调控多种细胞通路的关键蛋白,常被称为 “主控调节因子”。其中,转录因子 L(TF L)在神经分化、造血及器官发生等发育过程中作用关键,对维持干细胞多能性和中枢神经系统、眼部等组织的正常发育十分重要,其失调与相关难治性发育障碍密切相关,是潜在治疗靶点。
然而,TF L的表达与纯化(尤其全长形式或特定功能结构域)因蛋白结构复杂具有挑战性:其含LIM结构域、同源结构域及内在无序区域,在大肠杆菌中表达易错误折叠形成包涵体,复性条件难优化且功能蛋白得率低;昆虫细胞(Sf9)、哺乳动物细胞(HEK293、CHO)、酵母(毕赤酵母)等其他系统也存在得率不足、纯化复杂、蛋白降解等问题。这些难题严重限制了TF L的结构与功能研究,阻碍了靶向疗法研发。
本应用我们采用eProtein Discovery系统成功表达并纯化了全长TF L,以及一个未知功能结构域(L2)及其结合结构域(L3)。通过使用可溶性标签,以及富含锌离子(Zn²⁺)和二硫键形成剂的无细胞混合体系,我们优化了可溶性TF L蛋白的制备流程。利用标记488 Atto染料、含TF L结合位点的双链DNA,对纯化后蛋白的 DNA 结合功能进行了验证。研究结果不仅解决了TF L合成领域长期存在的技术难题,更为治疗性药物研发开辟了新路径,同时确立了eProtein Discovery系统作为复杂转录因子研究与制备领域变革性工具的核心地位。
二、工作流程
eProtein Discovery系统利用数字微流控技术,可自动筛选多种DNA 构建体(eGene构建体)和无细胞混合体系,优化可溶性目标蛋白的制备与纯化条件(图 1)。系统能在24小时内生成192组表达数据和30组纯化数据,这一快速筛选能力加速了蛋白放大生产最优条件的确定。仅需48小时,用户即可完成从DNA到可溶性、经纯化且可直接用于实验的蛋白制备,较大程度简化了生产流程,推动科研与治疗性蛋白研发的快速推进。
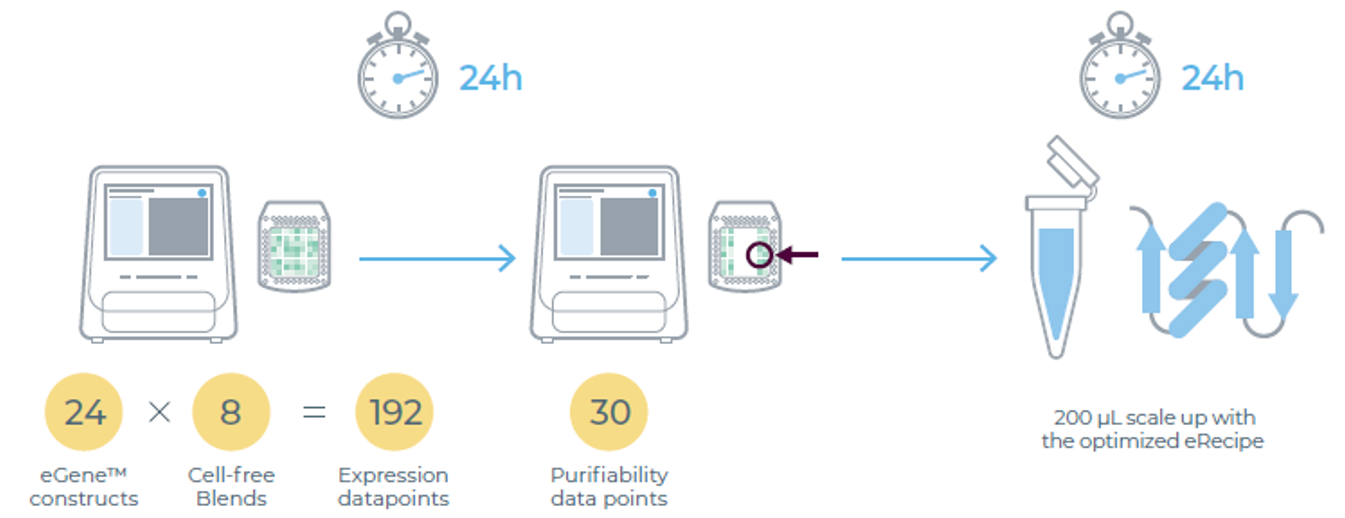
图1:eProtein Discovery系统流程图:48小时内完成从DNA到可直接用于实验的蛋白制备。
三、方法
1、eProtein Discovery系统筛选
本研究利用eProtein Discovery系统开展结构预测、实验运行、数据可视化及分析工作。样品制备采用可溶性标签筛选技术,将eGene构建体加载至eProtein Discovery筛选卡盒中完成。本研究选取了三种TF L变体(图 2):全长蛋白、未知功能结构域(L2)及 DNA 结合结构域(L3)。将这些变体导入eProtein Discovery云软件进行密码子优化后,在其两端添加3C和TEV序列。L2和L3变体的设计借助系统内置的 AlphaFold 结构预测工具,通过精准识别并分离TF L的重要功能区域完成。使用eGene制备试剂盒(可溶性标签筛选)构建含不同可溶性标签的表达载体,同时构建1个无可溶性标签的对照载体,最终获得24个 eGene构建体(图 3a)。每个构建体的C端均含链霉亲和标签(Strep-tag)(用于磁珠纯化)和检测标签(用于蛋白表达及纯化后的定量分析)。
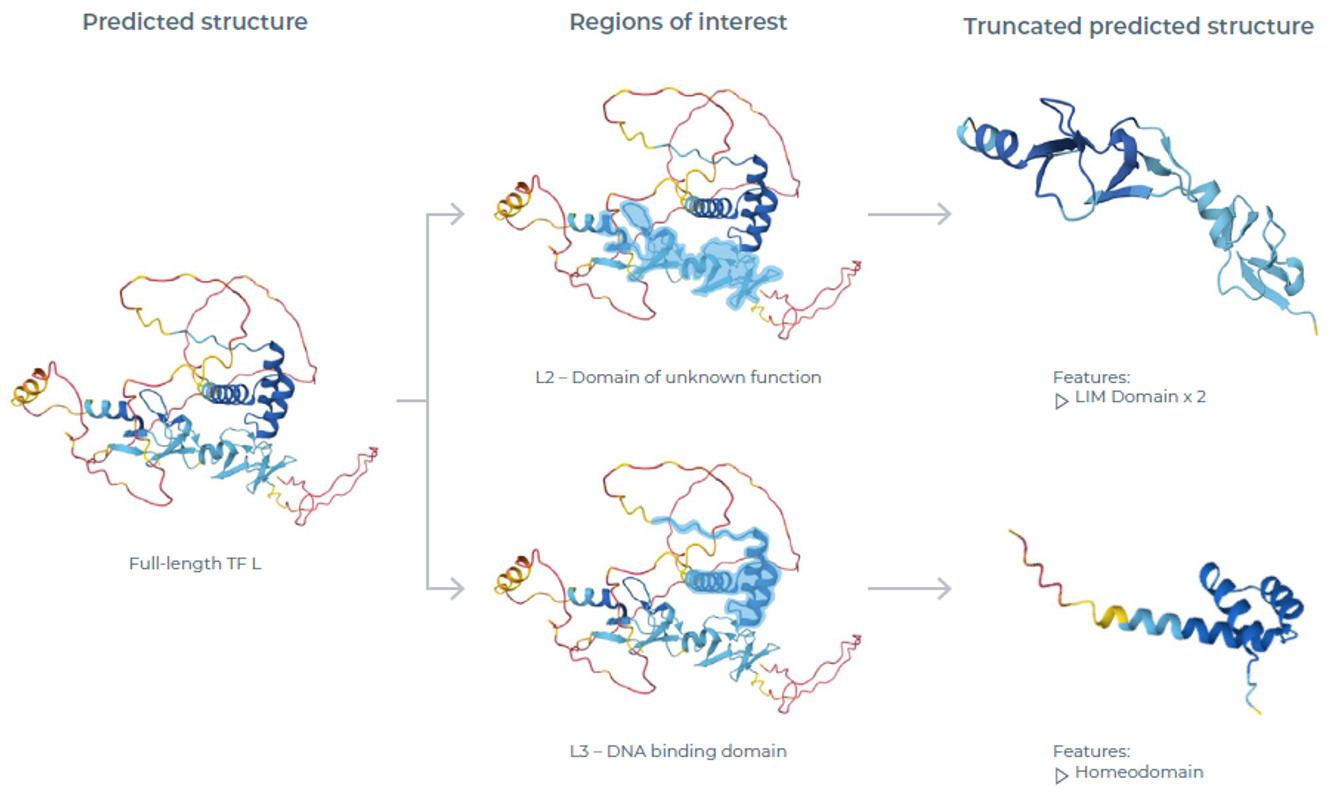
图2:TF L变体的AlphaFold结构预测。图示为全长TF L的预测结构(重点关注区域已高亮标注)。蛋白变体L2和L3基于上述区域筛选设计,同时获得了这些截短蛋白的结构预测结果。
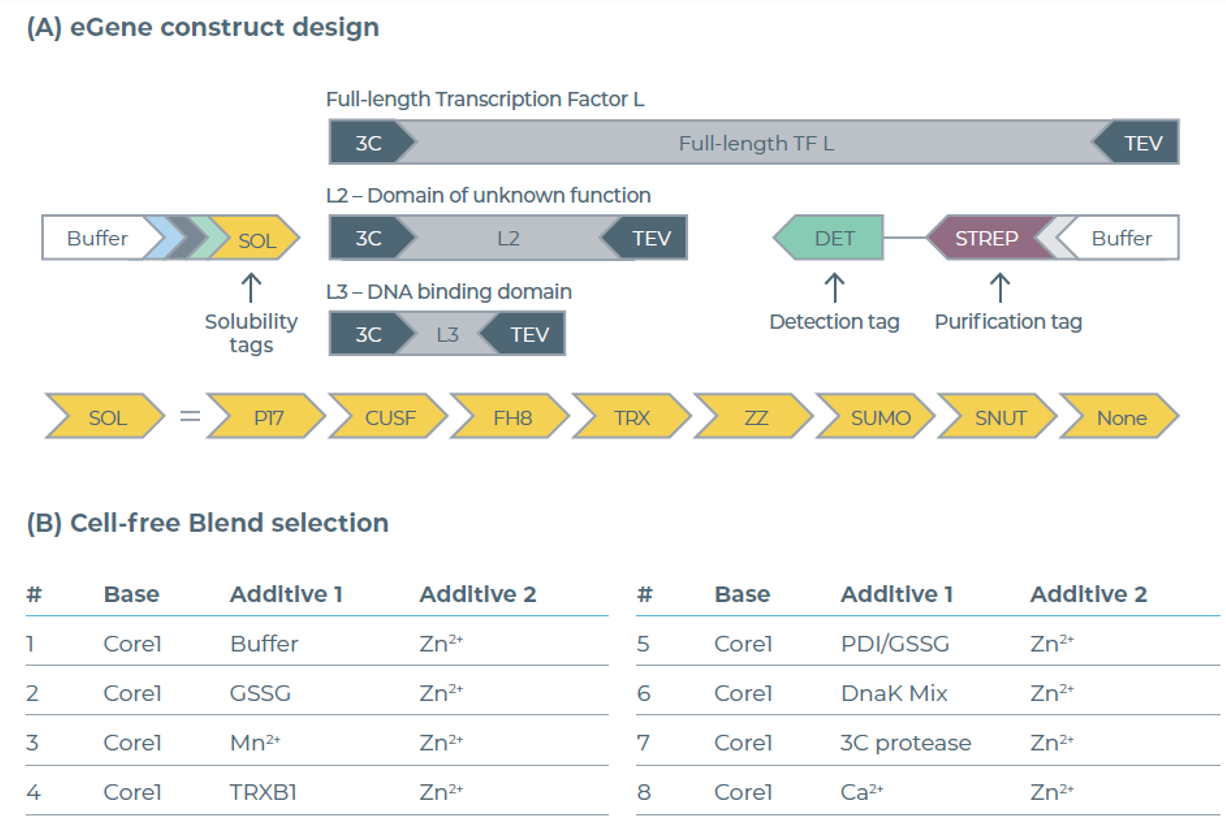
图3:eGene构建体与无细胞混合体系的筛选。(A) 含可溶性标签的TF L eGene构建体设计方案。(B) 用于提高可溶性蛋白得率的无细胞混合体系筛选结果。
本研究选取8种无细胞混合体系,其包含无细胞核心蛋白翻译机制,并添加了金属辅因子、分子伴侣(DnaK)、二硫键促进剂(PDI+/GSSG)及用于可溶性标签切除的 3C 蛋白酶(图 3b)。鉴于TF L含两个 LIM 结构域,特选用Zn²⁺,推测其可稳定TF L中这些富含半胱氨酸的锌结合区域。
将24个eGene构建体、8种无细胞混合体系,连同纯化磁珠、对照样品、空白样品及洗脱缓冲液一同加载至卡盒中。借助eProtein Discovery系统的自动化功能,该实验设置可生成并分析192组表达图谱。系统自动筛选出每种TF L变体对应的10组高表达eGene/无细胞混合体系组合用于纯化,并通过蛋白检测确定预测放大生产得率,上述所有流程均在24小时内完成。
2、放大生产蛋白质
针对每种TF L变体,选取预测纯化得率最高的无细胞表达组合进行过夜放大培养,采用放大生产专用试剂纯化,最终获得微克级目标蛋白。通过SDS-PAGE和Western blot实验,验证了蛋白的成功表达与纯化。
3、DNA 结合实验
通过DNA结合电泳迁移率变动分析(EMSA)评估蛋白的 DNA 结合能力并验证其正确折叠。将放大生产获得的TF L变体与Atto 488标记的双链DNA(dsDNA)共同孵育(该dsDNA通过退火含TF L结合位点的单链 DNA(ssDNA)制备)。样品在4–16%天然凝胶中电泳,通过与游离DNA探针对比评估迁移率变动。采用含突变TF L结合位点的阴性对照验证结合特异性。针对全长TF L,设置三个浓度梯度以探究蛋白浓度对DNA-TF L复合物形成的影响。
四、数据与讨论
eProtein Discovery系统在转录因子L(TF L)的全长蛋白、未知功能结构域(L2)及结合结构域(L3)的表达与纯化中展现出出色效率。该技术24小时内快速筛选192组表达条件,生成30组可纯化性数据。通过全面筛选,成功确定了可溶性功能性TF L变体的最优制备条件。如图 4 所示,已明确获得更高表达及纯化效果的可溶性标签与无细胞混合体系组合,凸显了该系统通过精准优化条件以实现更高得率和纯度的核心能力。
在筛选出的Top30表达条件中,所有构建体均含可溶性标签,凸显其在获得可溶性及可纯化蛋白得率中的关键作用。全长TF L和L2采用P17可溶性标签,L3采用CUSF标签,与无可溶性标签的构建体相比,蛋白表达量提升1.83倍。这一结果表明,该技术可通过策略性标签筛选优化表达效率,对需表达复杂难制备蛋白的研究人员而言是核心优势。
此外,无细胞混合体系的使用进一步提高了表达得率。每个体系均含Zn²⁺,其对稳定TF L中富含半胱氨酸的锌结合区域十分重要。添加GSSG使全长TF L的蛋白表达量提升约11%,而蛋白二硫键异构酶(PDI⁺)与 GSSG 的组合使L2和L3的表达量分别显著提升75%和47%(缓冲液 + Zn²⁺组数据未展示)。GSSG和PDI⁺/GSSG提供的氧化环境可维持半胱氨酸残基的氧化还原状态,进而支持蛋白正确折叠,这对TF L的结构完整性十分重要。尽管TF L本身不含二硫键,但维持适宜的氧化还原环境可避免异常相互作用(如半胱氨酸错配或蛋白聚集),确保LIM结构域中锌离子的正确配位。
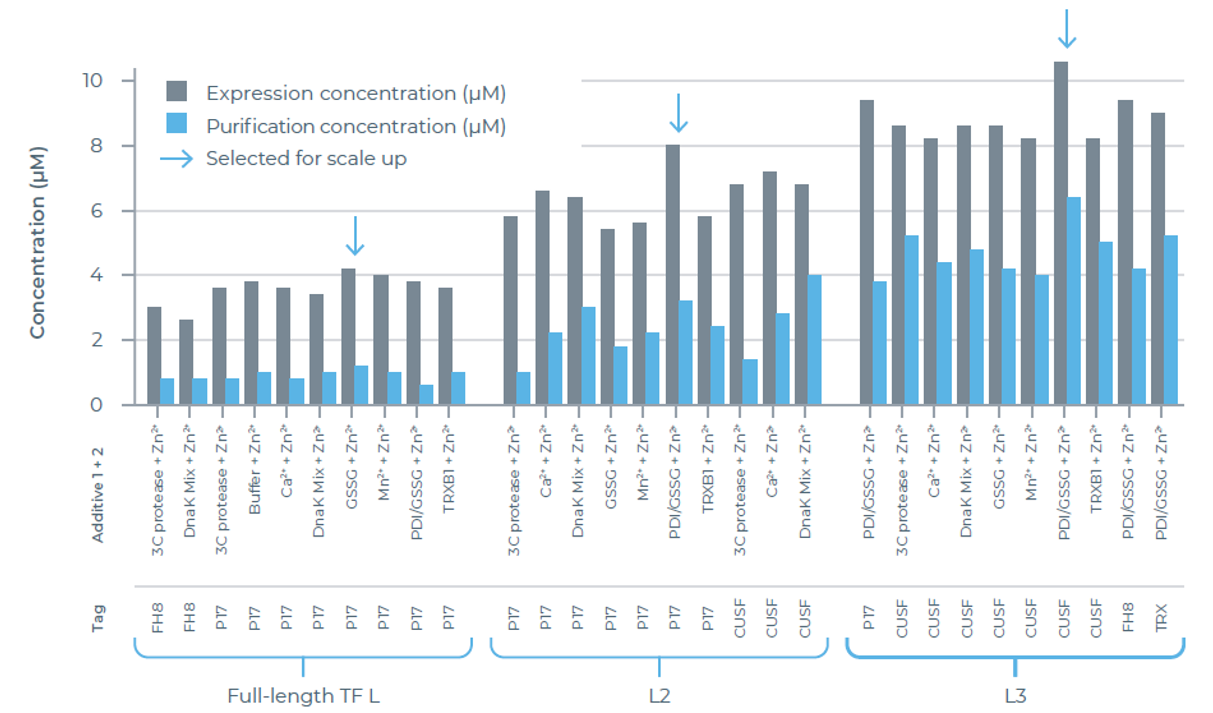
图4:TF L变体的表达与纯化结果。
将优化后的构建体和无细胞混合体系混合进行过夜放大培养,在1.5 mL离心管中获得微克级的各TF L变体蛋白。SDS-PAGE分析证实蛋白成功表达并纯化,考马斯亮蓝染色凝胶显示,洗脱泳道中出现与预期分子量一致的单一蛋白条带,表明纯化后蛋白纯度达标(图5)。通过抗Strep-tag II抗体验证了L2和L3变体C端链霉亲和标签(Strep-tag)的存在,证实完整蛋白序列已成功合成(图5)。
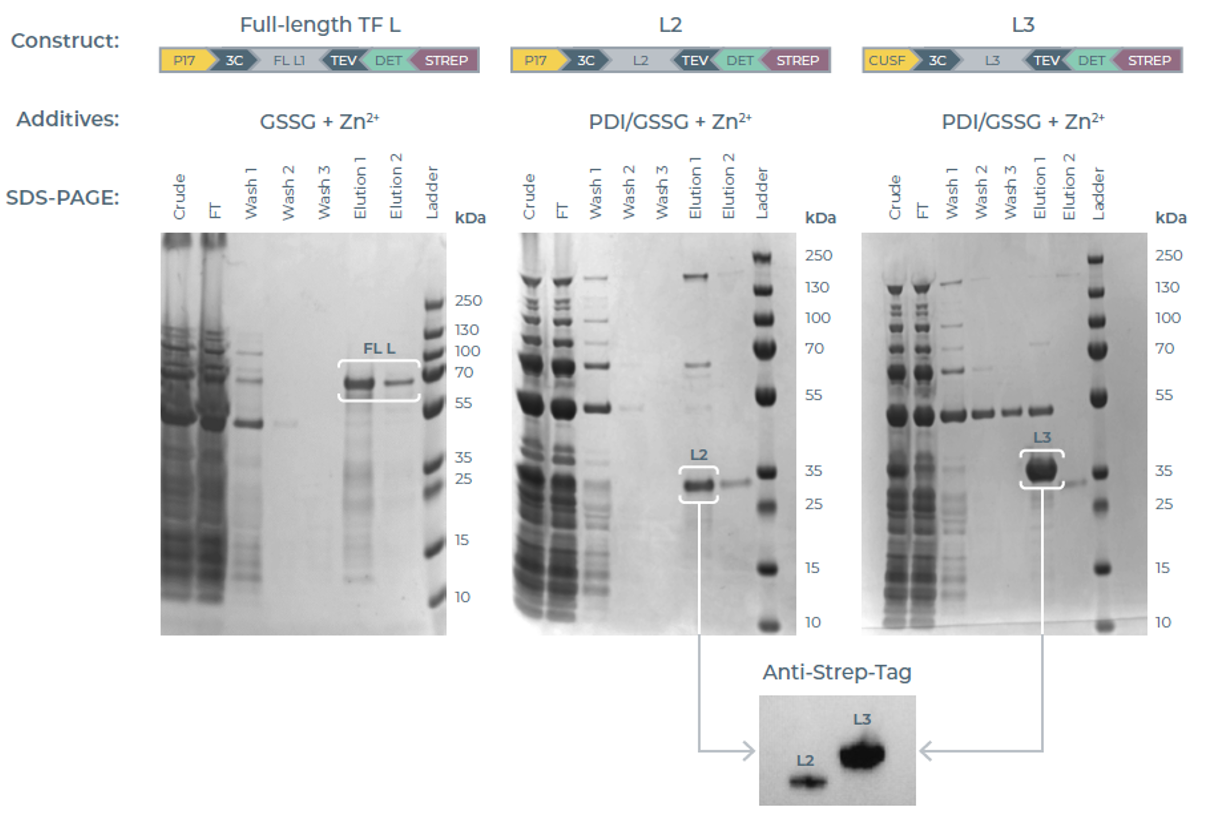
图5:放大生产结果。
为验证合成蛋白的功能,开展了DNA结合EMSA实验。结果证实,eProtein Discovery系统制备的蛋白保留了天然功能:全长TF L与含其结合位点的Atto 488标记 DNA 探针呈浓度依赖性结合,天然凝胶上可见清晰迁移率变动(图6A);L3结合结构域也成功与DNA探针形成复合物,而阴性对照(含突变TF L结合位点的 DNA)无结合现象,证实了相互作用的特异性(图6B)。值得注意的是,L2结构域未与DNA结合,提示其在TF L中可能承担其他结构或功能角色,这对TF L的调控活性可能十分重要。
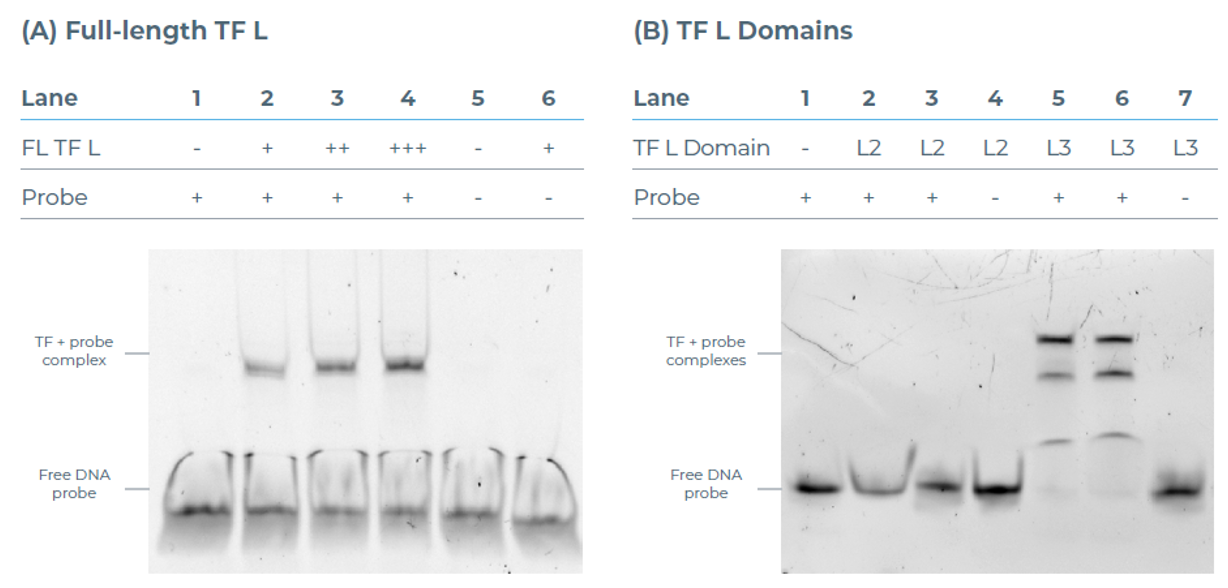
图6:DNA结合EMSA实验结果。(A) 不同浓度的全长TF L与含TF L结合位点的Atto 488标记双链DNA(dsDNA)孵育后,经天然凝胶分析的结果;采用含突变TF L结合位点的阴性对照探针验证结合特异性。(B) TF L未知功能结构域(L2)及结合结构域(L3)的 DNA 结合能力评估结果。
五、结论
eProtein Discovery 系统是攻克转录因子 L(TF L)表达与纯化难题的突破性工具,该蛋白对发育生物学和治疗创新十分重要。相较于传统方法易导致蛋白错折叠、得率低的问题,该系统借助数字微流控技术,能快速优化表达条件,48小时内即可提效制备高质量功能性蛋白,且经DNA结合实验证实其关键生物学功能得以保留。该系统为药物研发、再生医学及复杂蛋白研究提供了核心支撑,助力加速科研突破。
上海曼博生物是Nuclera品牌的官方代理商。如咨询产品信息,欢迎扫码添加小助手微信联系我们!



 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 













