
 发布时间:2025/08/21 点击数:593
发布时间:2025/08/21 点击数:593 一、TGF-β1有什么背景?什么用途?
转化生长因子-β1 (TGF-β1) 是TGF-β 超家族中的多效性细胞因子。TGF-β1 调节各种细胞过程,包括细胞增殖、生长、分化、运动和凋亡 [1]。它在免疫反应、组织修复和上皮-间质转化中重要的作用。转化生长因子-β1 由多种细胞类型产生,包括免疫细胞、成纤维细胞和上皮细胞。它以无活性或潜伏复合物的形式合成和分泌,与潜伏期相关蛋白 (LAP) 结合,并靶向细胞外基质 [2]。它由 TGF-β 激活剂(包括纤溶酶、基质金属蛋白酶、整合素)从潜伏期释放。一旦 LAP 裂解,成熟的转化生长因子-β1 就是由两个相同的亚基通过二硫键连接的同型二聚体蛋白质。其氨基酸序列由390个氨基酸组成。TGF-β1通过细胞表面受体复合物(包括TGF-βRII/TGF-βRI和ALK-5/ALK-1)发出信号。这引发下游信号级联,例如Smad依赖性通路和Smad非依赖性通路。
在细胞培养中,重组TGF-β1蛋白是许多胚胎干细胞和诱导性多能干细胞维持培养基中不可或缺的生长因子,包括常用的化学定义的E8、StemPro和mTeSR培养基[3–5]。转化生长因子-β1支持干细胞的存活和多能性的维持[1]。TGF-β1用于促进多种细胞类型的分化,例如成纤维细胞、上皮细胞和免疫细胞。它与其他生长因子(例如BMP-2)联合使用,可调节骨髓基质细胞分化,或与IL-2和IL-6联合使用,可调节Treg细胞和Th17细胞的分化[6–8]。
转化生长因子-β1 (TGF-β1) 是一种多效性细胞因子,调节多种细胞过程,包括细胞增殖、生长、分化、迁移和凋亡。它是许多胚胎和诱导性多能干细胞维持培养基(包括常用的 E8、StemPro 和 mTeSR 培养基)中所需的生长因子。TGF-β1 还能促进多种细胞类型的分化,例如成纤维细胞、上皮细胞和免疫细胞。
迄今为止,重组人TGF-β1仅通过哺乳动物细胞蛋白表达系统(HEK或CHO)生产,而内源性蛋白污染物、成本和无动物成分等因素均构成挑战。
二、从何获取好的TGF-β1蛋白?
Qkine致力于重新定义生长因子和细胞因子生化质量的行业标准,并推出了First个经过优化、无动物成分且具有高生物活性的重组人TGF-β1,货号Qk010。
这样做的好处:
1. 无动物成分,与化学定义的干细胞培养基兼容
2. 在iPSC培养表现出色,具有高多能性 (nanog) 标记表达
3. 高纯度、丰富的生化数据以及优秀的批间一致性,高度可重复
Qk010 TGF-β1 PLUS 是一种高纯度24 kDa 二聚体,包含优化的 TGF-β1 蛋白成熟结构域。Qkine的 TGF-β1 PLUS 蛋白已由英国剑桥的专业干细胞生物技术公司Stemnovate进行了多次的测试,以验证其是否能够维持iPSC多能性。
另外Qkine CGT等级的TGF-β1 PLUS现已推出,如果您有临床研究需求,也欢迎联系曼博生物。上海曼博生物是英国Qkine正式授权的指定代理商。
三、Qkine TGF-β1的好,何以见得?
1、活性
使用萤火虫荧光素酶报告基因检测法,在瞬时转染的HEK293T细胞中测定TGF-β1 PLUS活性。用不同梯度稀释的TGF-β1 PLUS处理细胞三次。测定萤火虫荧光素酶活性并进行标准化。EC50 = 34.8 pg/ml。数据来自Qk010批号#011。
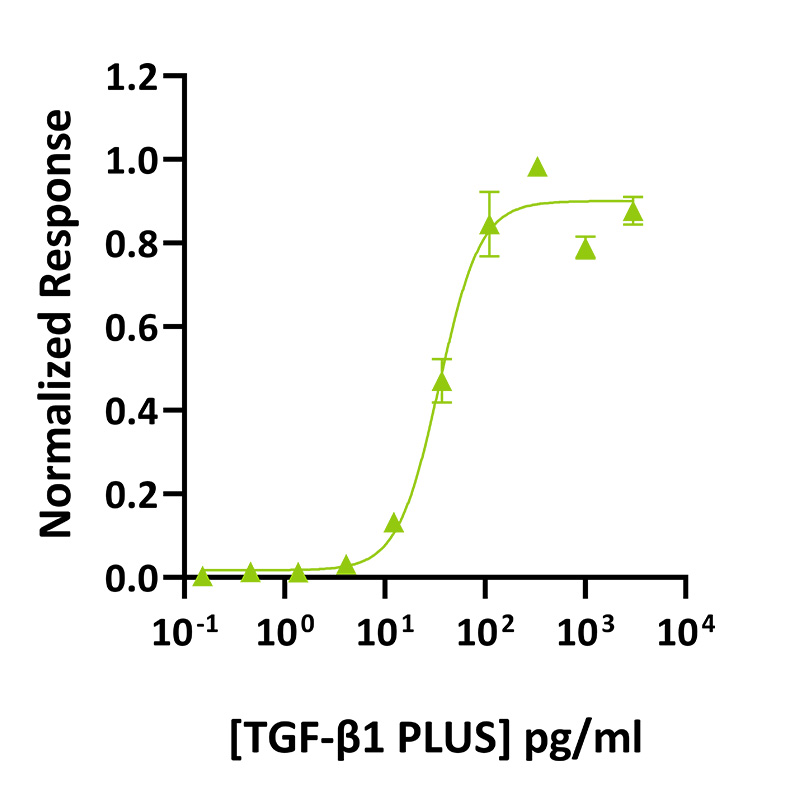
经检测,Qkine TGF-β1 PLUS 的生物活性优于其他供应商的 TGF-β1。使用 TGF-β1 反应性 (CAGA) 萤火虫荧光素酶报告基因,在瞬时转染的 HEK293T 细胞中测定生物活性。将细胞用梯度稀释的 TGF-β1 PLUS(Qk010,绿色)或来自两个其他供应商的 TGF-β1(黑色)处理 6 小时,重复三次。测量萤火虫荧光素酶活性,并将其与对照 Renilla 荧光素酶进行标准化。
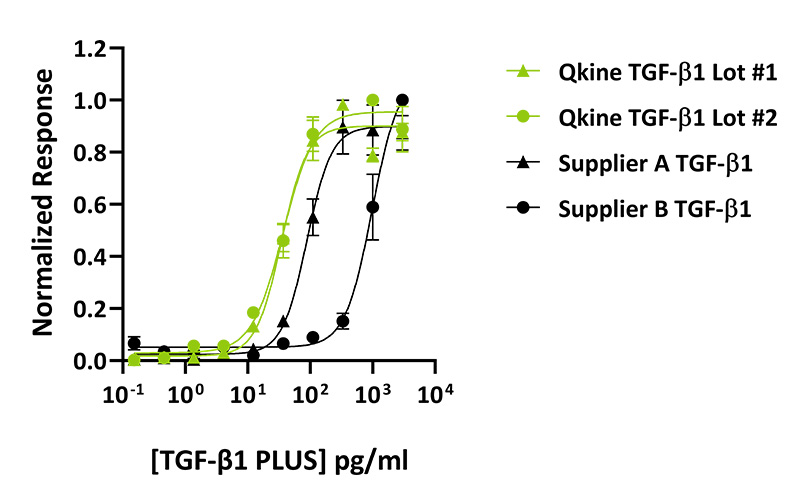
2、纯度
使用萤火虫荧光素酶报告基因检测法,在瞬时转染的HEK293T细胞中测定TGF-β1 PLUS活性。用不同梯度稀释的TGF-β1 PLUS处理细胞三次。测定萤火虫荧光素酶活性并进行标准化。EC50 = 34.8 pg/ml。数据来自Qk010批号#011。
TGF-β1 PLUS (Qk010) 二聚体在非还原性 (NR) 条件下以 24 kDa 的单一条带迁移,而在还原性 (R) 条件下以 13 kDa 的单体形式迁移。二聚体蛋白(生物活性形式)的产量高。纯化的重组蛋白 (7 μg) 在还原性 (+β-巯基乙醇,R) 和非还原性 (NR) 条件下使用 15% w/v SDS-PAGE 进行分离,并用考马斯亮蓝 R250 染色。数据来自Qk010批号#012。
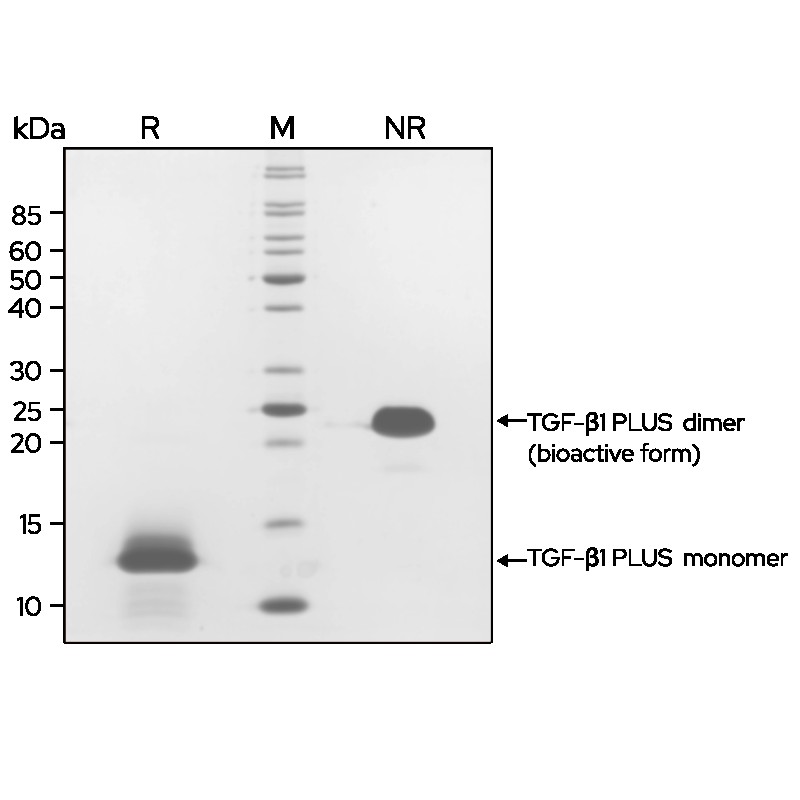
四、Qkine TGF-β1的特色应用及合作者数据
✅ 诱导多能干细胞和胚胎干细胞的分化和维持
✅ 化学定义的培养基优化素的替代
客户数据
1. 使用Qkine TGF-β1 PLUS (Qk010) 诱导iPSC衍生的中胚层祖细胞发生软骨分化而制成的软骨球体。数据由伦敦大学学院干细胞与再生医学系的Oliver Gardner /Valeriia Davydenko提供。
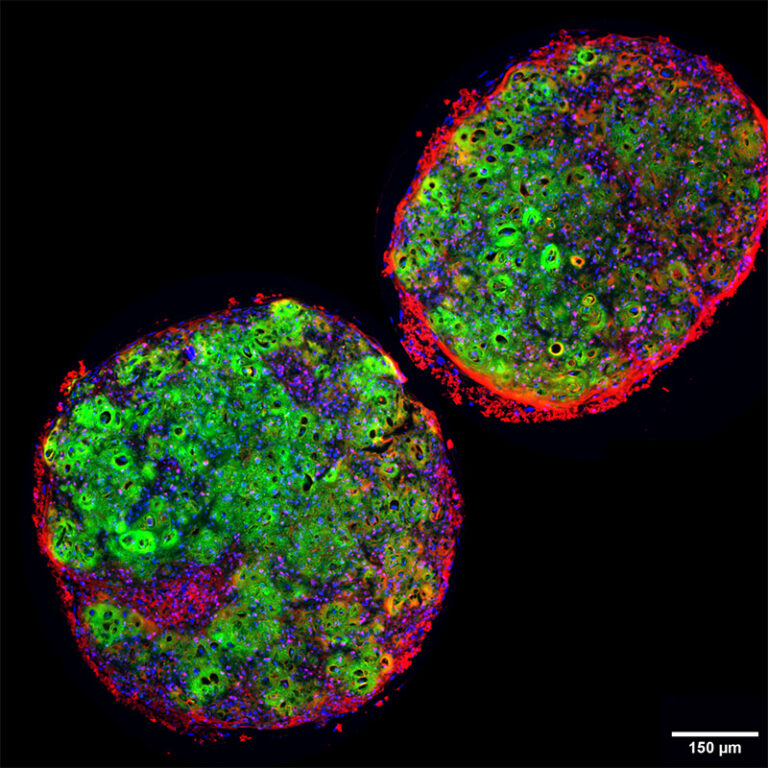
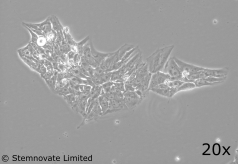
2. TGF-β1 PLUS (Qk010) 在含化学成分确定的血清和无饲养层的 iPSC 培养中,浓度为 1 ng/ml 时,仍能维持多能性和良好的菌落形态。TGF-β1 PLUS 的用量为 1 ng/ml;FGF-2 ( Qk025 ) 的用量为 100 ng/ml。数据来自Stemnovate。
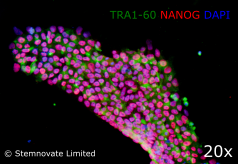
3. TGF-β1 PLUS在化学成分确定、无血清和无饲养层培养中高度有效维持 iPSC 多能性。多能性标志物 Tra 1-60 和 Nanog 的免疫染色检测显示,在含有 TGF-β1 PLUS (Qk010) 的确定成分培养基中,iPSC 系表达水平较高。在本研究中,Qkine TGF-β1 PLUS的表现优于Stemnovate常规使用的TGF-β1 。
五、总结概括
1. 高纯度优化TGF-β1蛋白(Uniprot:P01137)
2. 24 kDa(二聚体)
3. >98%,通过 SDS-PAGE 定量密度测定
4. 在大肠杆菌中表达
5. 无动物来源(AOF)和无载体蛋白
6. 在英国剑桥实验室制造
7. 乙腈、TFA 冻干
8. 以>50 µg/ml 的浓度重新悬浮于10mM HCl(重组溶液A)中,如有需要,添加载体蛋白,制备一次性使用试样并冷冻保存于 -20 °C(短期)或 -80°C(长期)
9. 替代蛋白质名称:Transforminggrowth factor-beta 1, TGF-beta 1, TGFβ1, TGFB1, TGF B1
10. 物种反应性:人类。物种相似性:鼠-99%;大鼠 -99%;牛 -100%;猪 -100%
11. 替代蛋白质:重组人TGF-β2蛋白(Qk072)12. 质谱法:具有预期质量的单一物种
13. 存储瓶回收率:>95%
14. 内毒素:<0.005 EU/μg 蛋白(低于检测水平)
使用Qkine重组人TGF-β1 PLUS蛋白 (Qk010) 的出版物
1. Modeling the selective growth advantage of genetically variant human pluripotent stem cells to identify opportunities for manufacturing process controlBeltran-Rendon C, Price CJ, Glen K et al.DOI: doi: 10.1016/j.jcyt.2024.01.010
2. Refined home-brew media for cost-effective, weekend-free hiPSC culture and genetic engineeringTruszkowski L, Bottini S, Bianchi S et al. DOI: https://doi.org/10.12688/openreseurope.18245.1
3. Recombinant production of growth factors for application in cell cultureVenkatesan M, Semper C, Skrivergaard S et al.DOI: doi: 10.1016/j.isci.2022.105054.
TGF-β1蛋白背景文献参考
[1] D. James, A. J. Levine, D. Besser, and A. Hemmati-Brivanlou, ‘TGFβ/activin/nodal signaling is necessary for the maintenance of pluripotency in human embryonic stem cells’, Development, vol. 132, no. 6, pp. 1273–1282, Mar. 2005, doi: 10.1242/dev.01706.
[2] J. P. Annes, J. S. Munger, and D. B. Rifkin, ‘Making sense of latent TGFβ activation’, J. Cell Sci., vol. 116, no. 2, pp. 217–224, Jan. 2003, doi: 10.1242/jcs.00229.
[3] J. Beers et al., ‘Passaging and colony expansion of human pluripotent stem cells by enzyme-free dissociation in chemically defined culture conditions’, Nat. Protoc., vol. 7, no. 11, pp. 2029–2040, 2012, doi: 10.1038/nprot.2012.130.
[4] T. E. Ludwig, V. Bergendahl, M. E. Levenstein, J. Yu, M. D. Probasco, and J. A. Thomson, ‘Feeder-independent culture of human embryonic stem cells’, Nat. Methods, vol. 3, no. 8, Art. no. 8, Aug. 2006, doi: 10.1038/nmeth902.
[5] A. Wang et al., ‘Induced Pluripotent Stem Cells for Neural Tissue Engineering’, Biomaterials, vol. 32, no. 22, pp. 5023–5032, Aug. 2011, doi: 10.1016 / j.biomaterials.2011.03.070.
[6] Y. Tang et al., ‘TGF-β1–induced migration of bone mesenchymal stem cells couples bone resorption with formation’, Nat. Med., vol. 15, no. 7, Art. no. 7, Jul. 2009, doi: 10.1038/nm.1979.
[7] M. Elsafadi et al., ‘Convergence of TGFβ and BMP signaling in regulating human bone marrow stromal cell differentiation’, Sci. Rep., vol. 9, no. 1, Art. no. 1, Mar. 2019, doi: 10.1038/s41598-019-41543-0.
[8] M. Veldhoen, R. J. Hocking, C. J. Atkins, R. M. Locksley, and B. Stockinger, ‘TGFβ in the Context of an Inflammatory Cytokine Milieu Supports De Novo Differentiation of IL-17-Producing T Cells’, Immunity, vol. 24, no. 2, pp. 179–189, Feb. 2006, doi: 10.1016/j.immuni.2006.01.001.


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 













