
 发布时间:2026/05/07 点击数:10
发布时间:2026/05/07 点击数:10 无细胞蛋白合成(cell free system)在复杂蛋白表达中的应用
摘要:无细胞蛋白合成(cell free system)因其开放、可调控、筛选效率高等特点,正在成为复杂蛋白表达与纯化优化的重要技术路径。本文围绕eProtein Discovery高通量蛋白表达筛选系统,结合添加剂组合优化与复杂转录因子TF L表达案例,系统解析无细胞系统如何通过可溶性标签、金属离子、分子伴侣、氧化还原调节剂等条件筛选,提高难表达蛋白的可溶性、纯化得率和功能活性,为复杂蛋白制备、结构功能研究与药物研发提供技术参考。
关键词:无细胞蛋白合成、无细胞蛋白表达、cell free system、无细胞系统、高通量蛋白表达筛选、全自动蛋白表达筛选、无细胞蛋白表达筛选、eProtein Discovery、蛋白表达优化、复杂蛋白制备、转录因子表达、可溶性标签、蛋白纯化
一、为什么复杂蛋白需要进行表达条件优化?
在蛋白质结构与功能研究中,不同蛋白对表达环境的需求差异很大。对于结构简单、稳定性较好的蛋白,传统大肠杆菌、昆虫细胞或哺乳动物表达体系通常可以满足基础制备需求。但对于结构复杂、折叠要求高、易聚集或依赖辅因子的蛋白,传统体系常常面临明显限制。
常见难点包括:
- 蛋白错误折叠,形成包涵体;
- 可溶性差,表达后难以纯化;
- 需要特定金属离子或辅因子才能维持结构;
- 含多个半胱氨酸或二硫键,对氧化还原环境敏感;
- 含内在无序区域,容易降解或聚集;
- 全长蛋白表达困难,只能获得截短片段;
- 纯化后功能活性不足,无法用于下游实验。
这些问题在转录因子、膜蛋白、金属酶、含二硫键蛋白、毒性蛋白、GPCR及其他复杂调控蛋白中尤其常见。
无细胞蛋白合成体系的优势在于,它不依赖完整细胞生长环境,而是在开放反应体系中完成蛋白合成。研究者可以根据目标蛋白特点,灵活调整反应条件,例如添加金属离子、辅因子、分子伴侣、氧化还原调节剂或标签切割酶,从而更快找到适合目标蛋白的表达环境。
这也是无细胞系统区别于传统表达体系的重要价值:它不是只提供一个固定表达环境,而是提供一个可以被快速筛选和调控的系统。
二、无细胞蛋白合成系统的筛选逻辑
eProtein Discovery系统将无细胞蛋白合成与数字微流控技术结合,可用于高通量蛋白表达筛选。系统支持多种DNA构建体与多种无细胞混合体系进行组合筛选,从而快速评估不同表达条件对蛋白可溶性、表达量、纯化能力及功能活性的影响。
其核心筛选逻辑包括:
- 设计多个目标蛋白构建体;
- 对构建体进行密码子优化;
- 引入不同可溶性标签;
- 搭配不同无细胞混合体系;
- 同步评估表达量、可溶性和纯化表现;
- 选择表现更优的组合进行放大制备;
- 对纯化蛋白进行SDS-PAGE、Western blot或功能实验验证。
系统可在较短时间内生成大量表达条件数据,用于判断目标蛋白适合哪类构建体、哪种标签、哪类添加剂组合以及哪种无细胞反应体系。
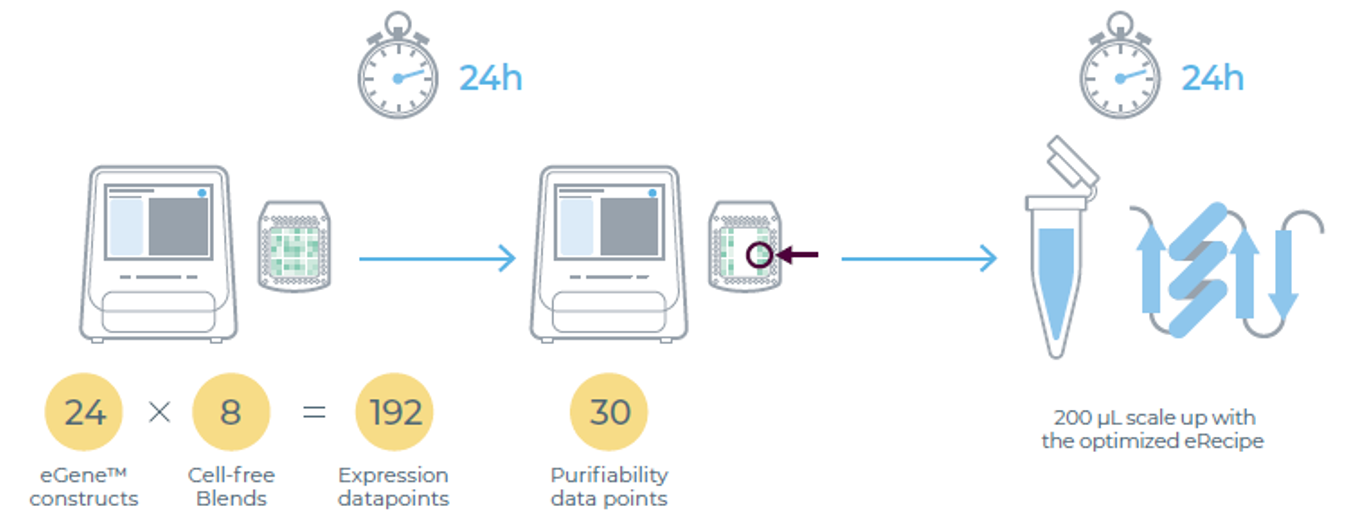
图1:eProtein Discovery系统流程图:48小时内完成从DNA到可直接用于实验的蛋白制备。
三、添加剂体系:无细胞系统优化复杂蛋白的关键
无细胞蛋白合成系统的重要优势之一,是可以根据目标蛋白结构特点加入不同添加剂。不同添加剂在蛋白折叠、活性维持、稳定性提升和可溶性改善方面发挥不同作用。
常见添加剂类型包括:
1. 金属离子
许多蛋白依赖金属离子维持结构或催化活性。相关研究中,约25%–50%的蛋白质属于金属结合蛋白。对于这类蛋白,金属离子不仅影响蛋白稳定性,也可能直接决定其是否具备酶活性。
常见金属离子包括:
- Zn²⁺
- Mn²⁺
- Ca²⁺
例如,Zn²⁺可用于稳定富含半胱氨酸的锌结合区域;Mn²⁺可作为部分酶类蛋白的关键辅因子;Ca²⁺则可能对某些蛋白的热稳定性产生积极影响。
2. 有机辅因子
部分酶类蛋白需要有机辅因子才能形成正确构象或发挥催化功能。若体系中缺少对应辅因子,即使蛋白成功表达,也可能无法获得理想活性。
常见有机辅因子包括:
- NAD
- PLP
- FAD
- Acetyl-CoA
- SAM
例如,PLP可参与转氨酶类蛋白的催化过程;NAD常与氧化还原酶类蛋白相关;SAM则与甲基转移过程有关。
3. 分子伴侣
分子伴侣可帮助新生肽链折叠,减少错误折叠和聚集。对于易聚集蛋白、结构复杂蛋白和多结构域蛋白,加入分子伴侣常常能改善可溶性表达结果。
常见分子伴侣包括:
- DnaK伴侣混合物
- TrxB1
4. 氧化还原调节剂
含半胱氨酸较多、存在二硫键或对氧化还原状态敏感的蛋白,往往需要合适的氧化还原环境。氧化还原调节剂可帮助维持半胱氨酸残基状态,降低错配、聚集或结构异常风险。
常见组合包括:
- GSSG
- PDI/GSSG
即使目标蛋白本身不形成典型二硫键,合适的氧化还原条件也可能帮助维持半胱氨酸相关结构区域的稳定性。
5. 标签切割酶
可溶性标签常用于提升蛋白表达和纯化效果,但在部分功能实验或结构研究中,需要去除标签。此时可加入3C蛋白酶等工具酶,用于标签切除。
四、添加剂组合筛选策略
在实际使用无细胞蛋白表达筛选系统时,添加剂并不是越多越好,而是需要根据目标蛋白特征进行合理组合。
常见判断逻辑如下:
- 含金属结合位点的蛋白:优先测试Zn²⁺、Mn²⁺、Ca²⁺等金属离子;
- 辅酶依赖型酶类:优先测试NAD、PLP、FAD等有机辅因子;
- 易聚集或折叠困难蛋白:优先搭配DnaK、TrxB1等分子伴侣;
- 含多半胱氨酸或二硫键相关蛋白:优先评估PDI/GSSG、GSSG等氧化还原体系;
- 需要去除可溶性标签的蛋白:可加入3C蛋白酶用于后续标签切除;
- 未知结构或复杂结构域蛋白:可通过多种构建体与多种无细胞混合体系组合筛选。
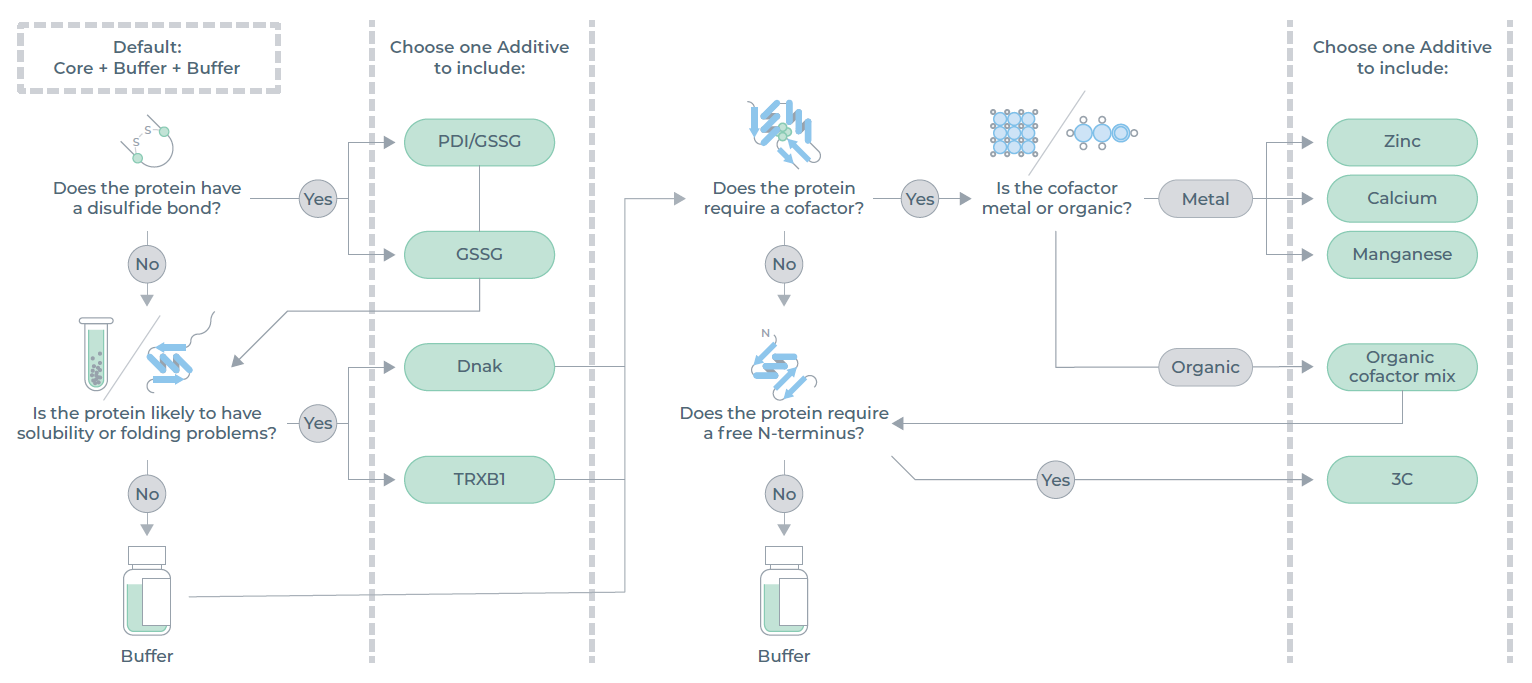
图2:添加剂指导决策树。每种表达用无细胞混合物中至多可添加两种添加剂。
五、案例背景:复杂转录因子TF L的表达挑战
转录因子是调控多种细胞通路的关键蛋白,常被称为“主控调节因子”。其中,转录因子L(TF L)在神经分化、造血及器官发生等发育过程中发挥重要作用,对维持干细胞多能性,以及中枢神经系统、眼部等组织正常发育十分关键。
但TF L的表达与纯化具有明显挑战,尤其是全长形式或特定功能结构域,常规体系中并不容易获得高质量蛋白。
其主要困难包括:
- 含LIM结构域;
- 含同源结构域;
- 存在内在无序区域;
- 在大肠杆菌中容易错误折叠形成包涵体;
- 复性条件难以优化;
- 功能蛋白得率较低;
- 在昆虫细胞、哺乳动物细胞和酵母体系中也可能出现得率不足、纯化复杂或蛋白降解问题。
这些问题会限制TF L的结构研究、功能验证和靶向药物开发。
在该案例中,研究采用eProtein Discovery系统表达并纯化了三类TF L变体:
- 全长TF L;
- 未知功能结构域L2;
- DNA结合结构域L3。
并通过可溶性标签、Zn²⁺、GSSG、PDI/GSSG等无细胞混合体系优化表达条件,最终获得可用于功能验证的蛋白样品。
六、构建体设计与结构预测
本研究将三种TF L变体导入eProtein Discovery云软件进行密码子优化,并在两端添加3C和TEV序列。L2和L3变体的设计借助系统内置AlphaFold结构预测工具完成,通过识别并分离TF L的重要功能区域,设计用于表达筛选的不同截短蛋白。
每个构建体的C端均包含:
- Strep-tag:用于磁珠纯化;
- 检测标签:用于蛋白表达及纯化后的定量分析。
最终构建了24个eGene构建体,包括多个含不同可溶性标签的表达载体,以及1个无可溶性标签对照载体。
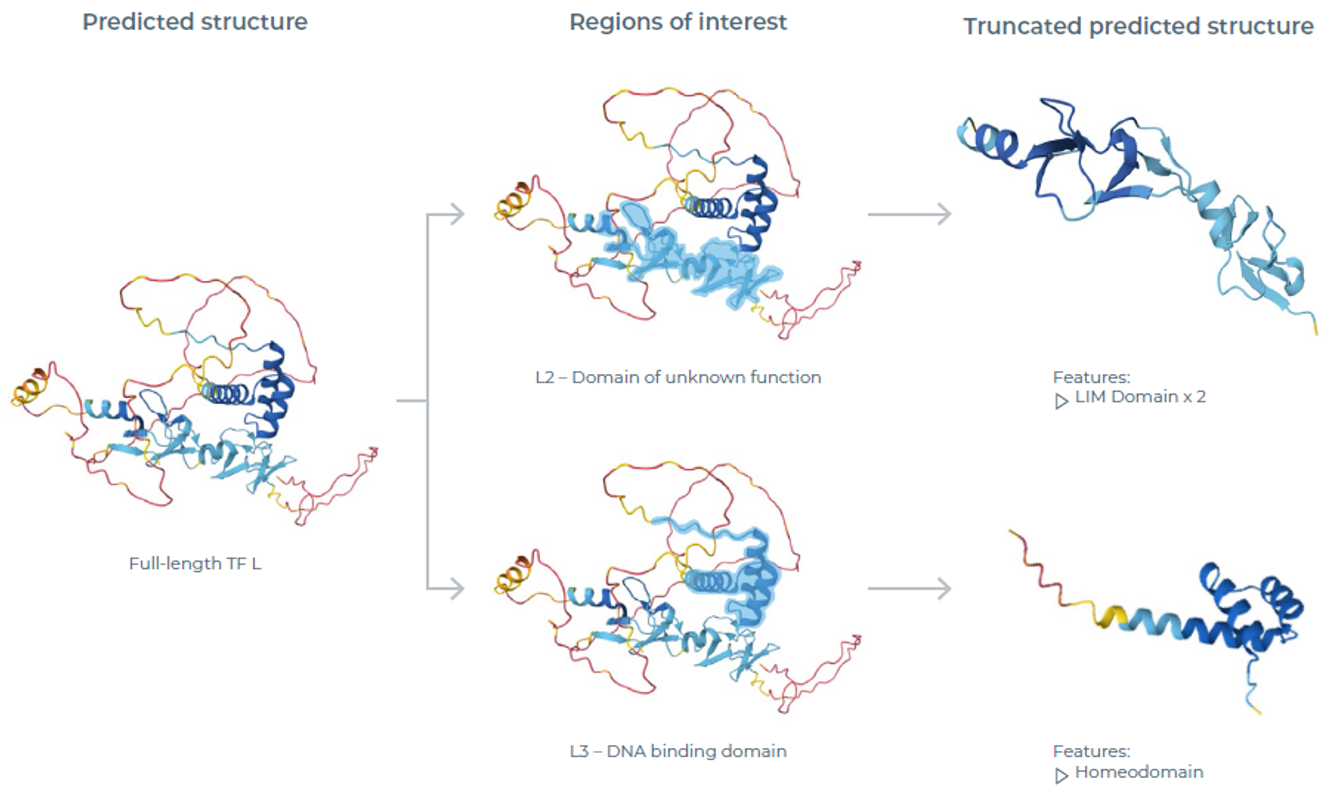
图3:TF L变体的AlphaFold结构预测。图示为全长TF L的预测结构,重点关注区域已高亮标注。蛋白变体L2和L3基于上述区域筛选设计,同时获得这些截短蛋白的结构预测结果。
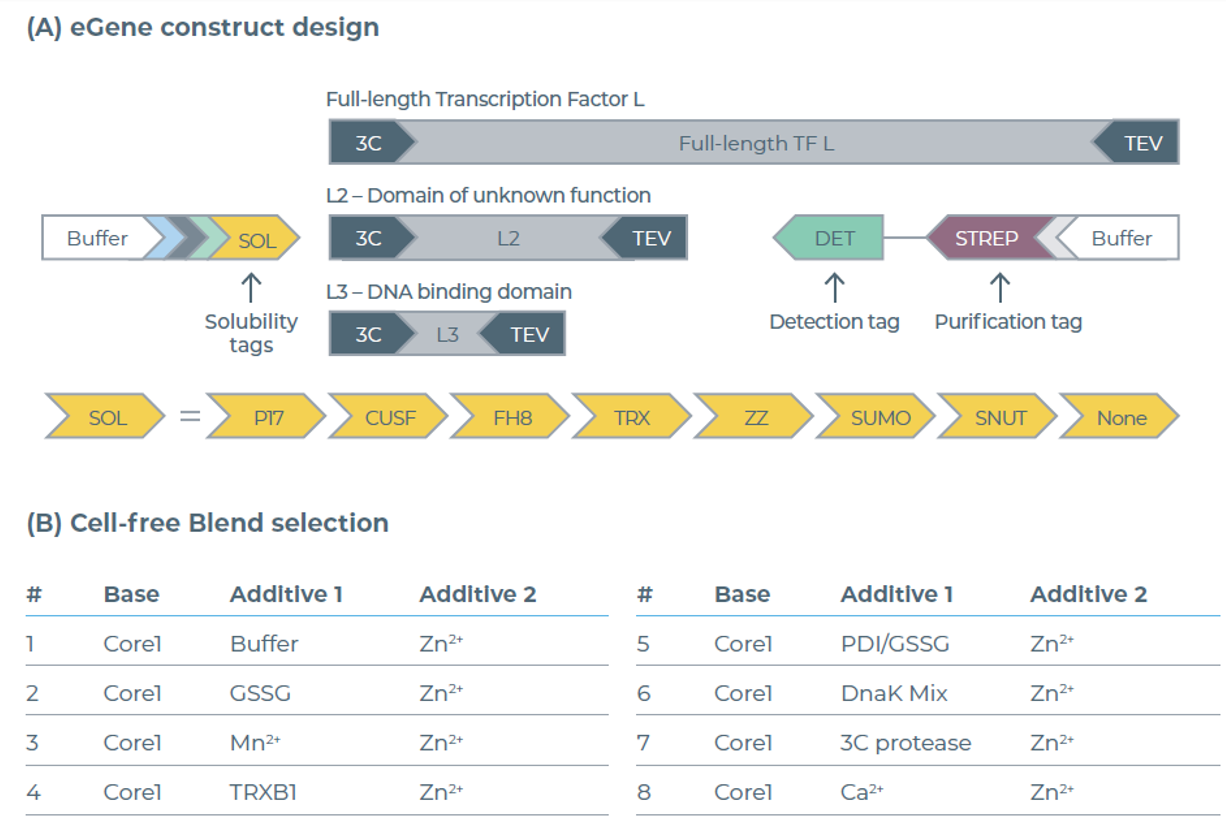
图4:eGene构建体与无细胞混合体系筛选。(A)含可溶性标签的TF L eGene构建体设计方案。(B)用于提高可溶性蛋白得率的无细胞混合体系筛选结果。
七、无细胞混合体系设计
本研究选取8种无细胞混合体系。这些体系包含无细胞核心蛋白翻译机制,并额外加入不同功能添加剂,包括:
- 金属辅因子;
- 分子伴侣DnaK;
- 二硫键促进剂PDI+/GSSG;
- 用于可溶性标签切除的3C蛋白酶。
由于TF L含有两个LIM结构域,因此特别选用Zn²⁺作为关键添加剂,用于稳定TF L中富含半胱氨酸的锌结合区域。
实验中,将24个eGene构建体与8种无细胞混合体系,连同纯化磁珠、对照样品、空白样品和洗脱缓冲液一同加载至卡盒中。借助系统自动化功能,该实验设置可生成并分析192组表达图谱。
系统会自动筛选每种TF L变体对应的10组高表达eGene/无细胞混合体系组合,用于后续纯化,并通过蛋白检测确定预测放大生产得率。上述流程均可在24小时内完成。
这种筛选方式的价值在于,它可以在短时间内同时评估多个关键变量,包括:
- 构建体长度;
- 可溶性标签类型;
- 无细胞混合体系;
- 添加剂组合;
- 纯化可行性;
预测放大得率。
八、放大生产与蛋白纯化
针对每种TF L变体,研究选取预测纯化得率最高的无细胞表达组合进行过夜放大培养,并采用放大生产专用试剂纯化,最终获得微克级目标蛋白。
后续通过SDS-PAGE和Western blot实验验证蛋白表达与纯化情况。
在放大生产中,关键观察点包括:
- 蛋白条带是否与预期分子量一致;
- 洗脱组分中是否出现目标蛋白;
- 纯化后是否存在明显杂带;
- Strep-tag是否完整;
- 截短结构域是否成功表达;
- 全长蛋白是否保留预期结构区域。
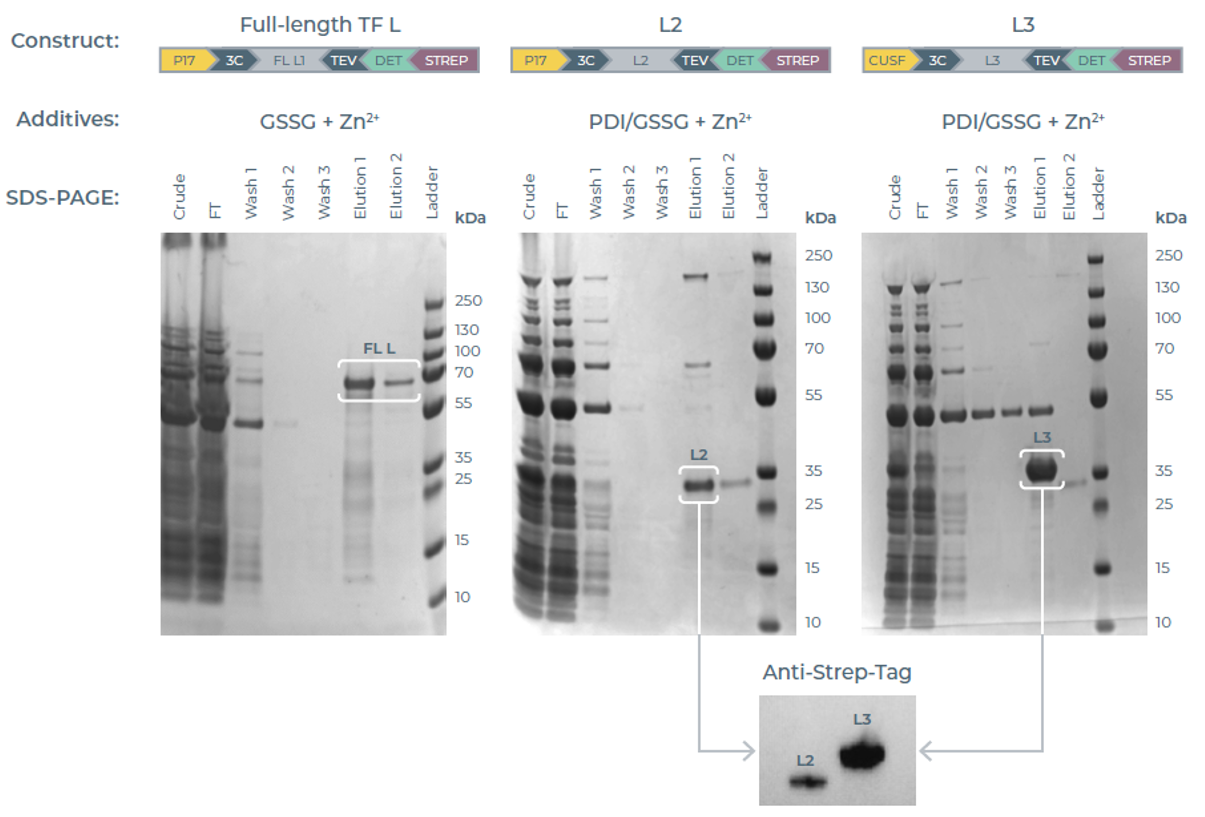
图5:eProtein Discovery系统放大生产结果。
九、表达筛选结果:可溶性标签与无细胞混合体系的影响
eProtein Discovery系统在TF L全长蛋白、L2结构域及L3结合结构域的表达与纯化中展现出较高筛选效率。系统在24小时内筛选192组表达条件,并生成30组可纯化性数据,从而快速确定可溶性功能性TF L变体的优选制备条件。
在筛选出的Top30表达条件中,所有构建体均含可溶性标签,说明可溶性标签在获得可溶性及可纯化蛋白方面发挥了关键作用。
具体结果包括:
- 全长TF L和L2采用P17可溶性标签;
- L3采用CUSF标签;
- 与无可溶性标签构建体相比,蛋白表达量提升1.83倍。
这一结果说明,对于复杂转录因子这类难表达蛋白,可溶性标签不仅是纯化辅助工具,也可能直接影响蛋白折叠路径、可溶性表达比例和最终可纯化得率。
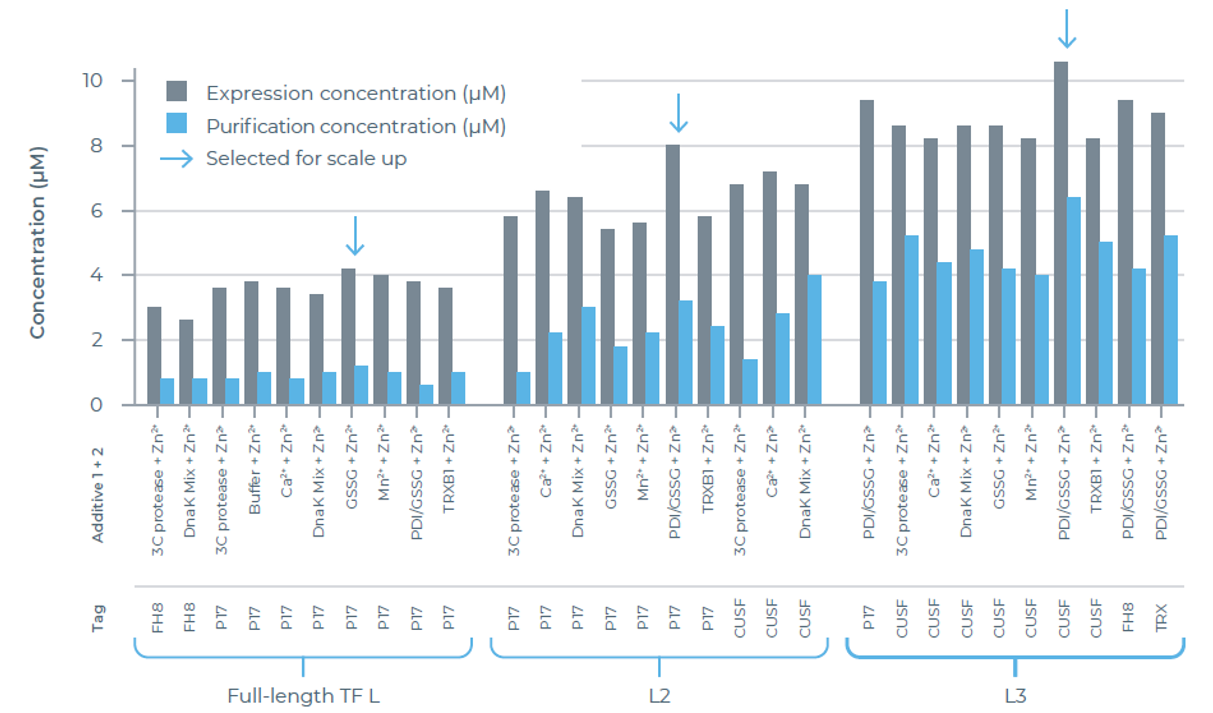
图6:TF L变体的表达与纯化结果。
十、Zn²⁺与氧化还原体系对TF L表达的影响
除可溶性标签外,无细胞混合体系的组成也显著影响表达结果。每个优选体系均含Zn²⁺,这对稳定TF L中富含半胱氨酸的锌结合区域十分重要。
添加GSSG后,全长TF L蛋白表达量提升约11%。而PDI⁺与GSSG组合对L2和L3的提升更明显:
- L2表达量提升75%;
- L3表达量提升47%。
GSSG和PDI⁺/GSSG提供的氧化环境,可帮助维持半胱氨酸残基的氧化还原状态,支持蛋白正确折叠。虽然TF L本身不含典型二硫键,但合适的氧化还原环境仍能减少异常相互作用,例如半胱氨酸错配、非特异性聚集或结构域不稳定。
对于LIM结构域这类富含半胱氨酸、依赖金属离子配位的区域,Zn²⁺和氧化还原条件的组合尤为关键。若氧化还原环境不合适,可能影响半胱氨酸状态,进而影响锌离子配位和结构域稳定性。
这一结果说明,无细胞蛋白合成体系并不是简单“表达蛋白”,而是可以通过反应体系设计,针对目标蛋白的结构特性进行定制化优化。
十一、EMSA实验:验证蛋白DNA结合功能
获得可溶性蛋白并不代表蛋白一定具备正确功能。因此,本案例进一步采用DNA结合电泳迁移率变动分析(EMSA)评估蛋白的DNA结合能力,并验证其折叠状态。
实验设计如下:
- 使用放大生产获得的TF L变体;
- 与Atto 488标记的双链DNA共同孵育;
- 该双链DNA由含TF L结合位点的单链DNA退火获得;
- 样品在4–16%天然凝胶中电泳;
- 通过与游离DNA探针对比评估迁移率变化;
- 设置含突变TF L结合位点的阴性对照验证结合特异性;
- 对全长TF L设置三个浓度梯度,观察蛋白浓度对DNA-TF L复合物形成的影响。
结果显示,全长TF L与含结合位点的Atto 488标记DNA探针呈浓度依赖性结合,在天然凝胶上出现清晰迁移率变化。L3结合结构域也能够与DNA探针形成复合物,而含突变结合位点的阴性对照无明显结合,证实相互作用具有特异性。
值得注意的是,L2结构域未与DNA结合,提示其可能承担非DNA结合相关的结构或调控功能。这一结果也符合结构域功能拆分的实验逻辑:L3更可能直接参与DNA结合,而L2可能参与蛋白稳定、构象调节、复合物形成或其他调控活动。
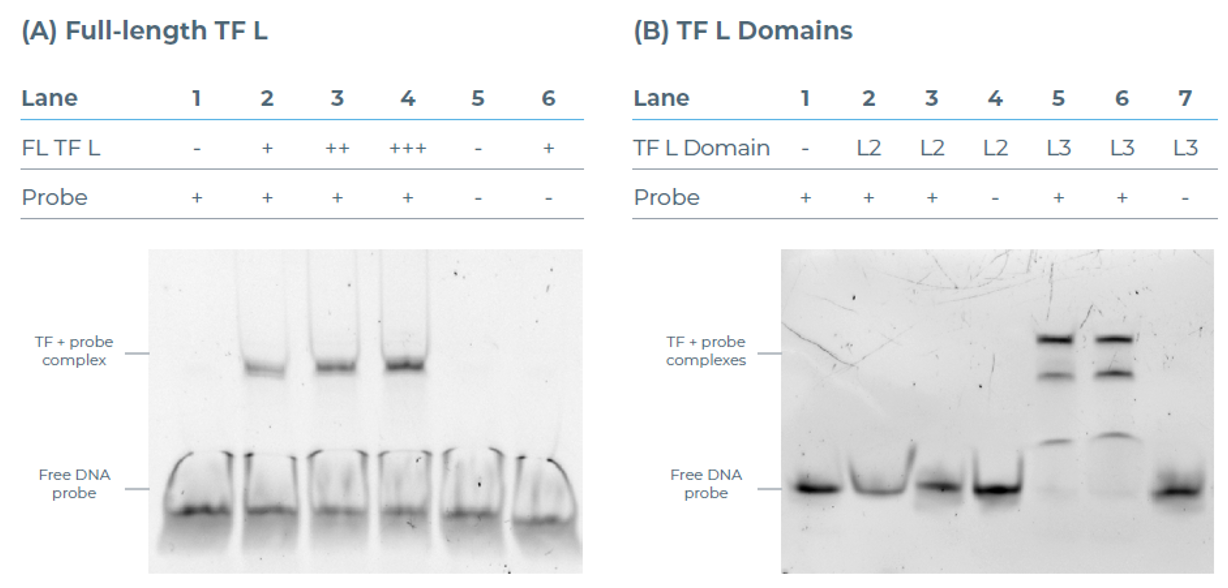
图7:DNA结合EMSA实验结果。(A)不同浓度全长TF L与含TF L结合位点的Atto 488标记双链DNA孵育后,经天然凝胶分析的结果;采用含突变TF L结合位点的阴性对照探针验证结合特异性。(B)TF L未知功能结构域L2及结合结构域L3的DNA结合能力评估结果。
十二、从案例看无细胞系统的技术价值
从TF L案例可以看出,无细胞蛋白合成体系的价值不只是“缩短表达时间”,更重要的是能够把表达优化过程变成可数据化、可组合筛选的系统工程。
对于复杂蛋白而言,传统表达体系经常需要逐一尝试不同载体、菌株、诱导温度、培养基、表达时间和纯化条件,周期较长且试错成本高。而无细胞系统可以直接围绕构建体、标签和反应体系进行并行筛选,快速判断哪一类组合更适合目标蛋白。
其优势主要体现在:
- 筛选速度快:短时间内完成多组条件并行比较;
- 变量可控:添加剂、标签和构建体均可系统设计;
- 适合复杂蛋白:对折叠困难、易聚集、结构域复杂蛋白更友好;
- 可直接连接功能验证:放大后蛋白可用于EMSA等下游实验;
- 有助于减少盲目试错:通过数据确定优选表达策略;
适配药物研发早期阶段:可更快获得靶蛋白用于结构、功能或筛选研究。
十三、结论
无细胞蛋白合成体系为复杂蛋白制备提供了一种高效、灵活且可调控的技术路径。通过eProtein Discovery这类高通量蛋白表达筛选系统,研究者可以在较短时间内系统评估DNA构建体、可溶性标签、无细胞混合体系和添加剂组合对蛋白表达、纯化及功能活性的影响。
在添加剂优化方面,金属离子、有机辅因子、分子伴侣和氧化还原调节剂可分别针对不同类型蛋白发挥作用;在TF L案例中,可溶性标签、Zn²⁺以及GSSG/PDI⁺体系共同改善了复杂转录因子的表达与纯化表现,并通过EMSA实验验证了蛋白保留DNA结合功能。
对于金属结合蛋白、含半胱氨酸结构域蛋白、转录因子、膜蛋白、易聚集蛋白及其他传统体系难表达蛋白,无细胞系统不仅能够提高表达筛选效率,也能为后续功能验证和药物研发提供更高质量的蛋白样品。
本文基于cell-free、无细胞蛋白表达、无细胞蛋白合成的应用文章、文献等公开技术资料由中国无细胞蛋白表达相关应用解决方案提供商上海曼博生物整理,仅用于科研信息分享。上海曼博生物可提供eProtein Discovery高通量无细胞蛋白表达筛选系统、cell free system蛋白表达解决方案及复杂蛋白制备相关产品与技术支持。


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 















