
 发布时间:2026/04/24 点击数:764
发布时间:2026/04/24 点击数:764 一、MSC、EVs和衰老背后的生物学
《传道书》中的智者曾感叹:“日光之下并无新事。”然而,有一件事在千百年来始终未曾改变,那就是人类渴望延缓衰老和死亡的步伐。或许我们无法阻止衰老的发生,但至少可以减少因衰老而带来的疾病和痛苦。现代医学和科技的进步为这一目标提供了希望,尤其是间充质干细胞(MSCs)在衰老研究中的潜力,成为了当下的研究热点。
间充质干细胞(MSCs)是多能干细胞,能够分化为骨细胞、脂肪细胞、软骨细胞,甚至可能分化为其他几种细胞类型。
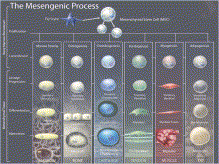
图1. The Mesengenic Process。间充质发生过程,阐释间充质干细胞(MSC)可以被诱导进入几种不同间充质谱系路径中。图片来源于文章DOI 10.1016/j.stem.2011.06.008
MSCs 具有较强的自我更新能力,并能进行多轮细胞分裂,这些干细胞储存在人体内,直到因受伤或疾病的需要被召回并“激活”。一旦被激活,MSCs 会参与修复过程,填补受损的血管,向疲惫的修复细胞捐赠线粒体,并分化为骨、软骨、脂肪或成纤维细胞。这些细胞的分泌物(secretomes)包括细胞因子、生长因子和细胞外囊泡(EVs,尤其是外泌体),这些成分具有抗炎作用和促血管生成作用,能够引导一系列有序的创伤修复和再生细胞活动。

图2. 间充质干细胞具有免疫调节和营养支持作用。图片来源于文章DOI 10.1016/j.stem.2011.06.008
随着年龄的增长,人体内的细胞逐渐受损,尤其是基因组和线粒体等结构的退化。细胞会随着时间的推移逐渐积累损伤,导致功能的下降,直到触发细胞的凋亡。衰老细胞常被称为“僵尸细胞”,它们会分泌与衰老相关的因子,促进局部的炎症反应和纤维化,影响周围健康细胞的功能。近年来的研究发现,去除这些衰老细胞或清除它们的分泌因子,甚至通过引入新的年轻或健康的细胞来替代受损细胞,可能成为减缓衰老相关慢性疾病发展的有效策略。
间充质干细胞(MSCs)正是这种潜力的体现。MSCs 对组织培养的适应性和自身的强韧性,使其成为理想的支持细胞,能够在多细胞类型的组织工程支架中发挥重要作用,例如用于心肌、肝脏、角膜、气管、主动脉及皮肤等多种组织的修复和再生。通过 MSCs 和它们的分泌物,或许能在不改变生物学极限的情况下,减缓衰老进程,延缓衰老相关疾病的发生。
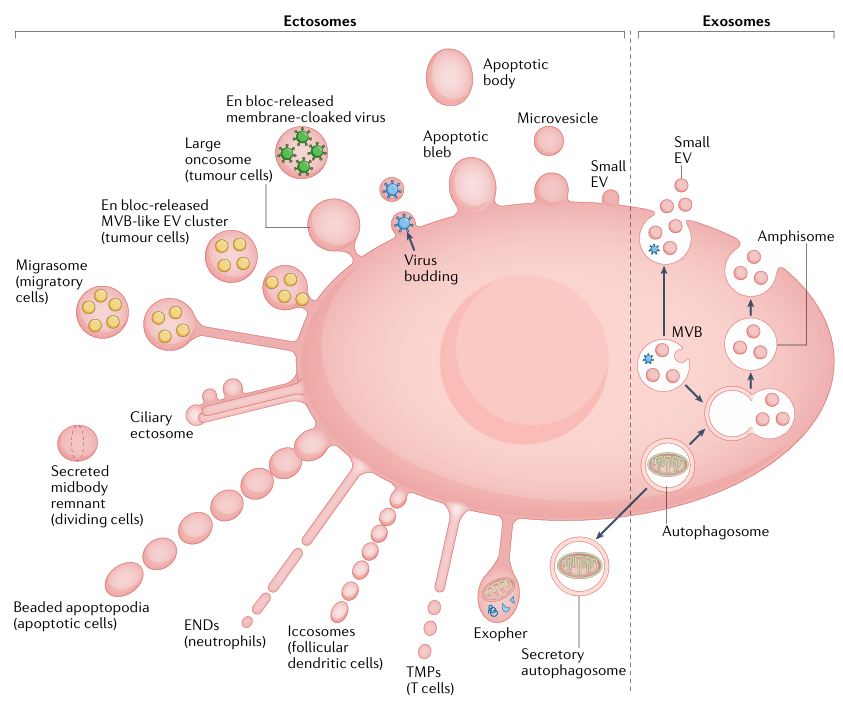
图3. 细胞外囊泡(EVs)的异质性。细胞外囊泡(EVs)是异质的、由磷脂膜包裹的结构。根据其生物发生机制,主要将EVs分为两种类型,分别为外泌体(exosomes)和外源性囊泡(ectosomes)。详情可参考原文:https://doi.org/10.1038/ s41577-022-00763-8
二、大规模EVs制造探索
近年来,hMSC-EVs 的需求急剧增加,突显了对可放大生物反应器的大规模生物制造的需求。然而,EVs 的生物发生过程对体外培养微环境敏感。接下来小编将分享一篇近期的研究,主题是关于 “不同培养方式下的外泌体生产效率研究、以及EVs质量和功能如何”的研究。这里可以将MSCs分泌的EVs理解为“小包裹”,里面装着脂质、蛋白质、核酸等这些对身体有用的 “治疗物质”。 但之前的问题是:这种 “小包裹” 产量太低,没法满足临床治疗的需求,所以需要找到能 “大规模生产” 它们的方法。

1、不同培养方式下的EVs生产效率研究
研究团队找了4种不同的 “培养方式”,来养脂肪来源间充质干细胞,看看哪种能产出更多、更好的EVs:
2D 平面培养:就像在孔板里养细胞,是以前常用的方式;
ULA 3D静态聚集体培养:在特殊盘子里让细胞聚成团养,但不怎么动;
SFB 动态3D培养(微载体依赖):一种能旋转的设备,让细胞在里面动态培养;
VWBR 动态3D培养(聚集体,无微载体):搅拌机制优化的动态设备,提供相对温和均匀可控的流体动力学环境,让细胞在更舒适的体外环境中培养。
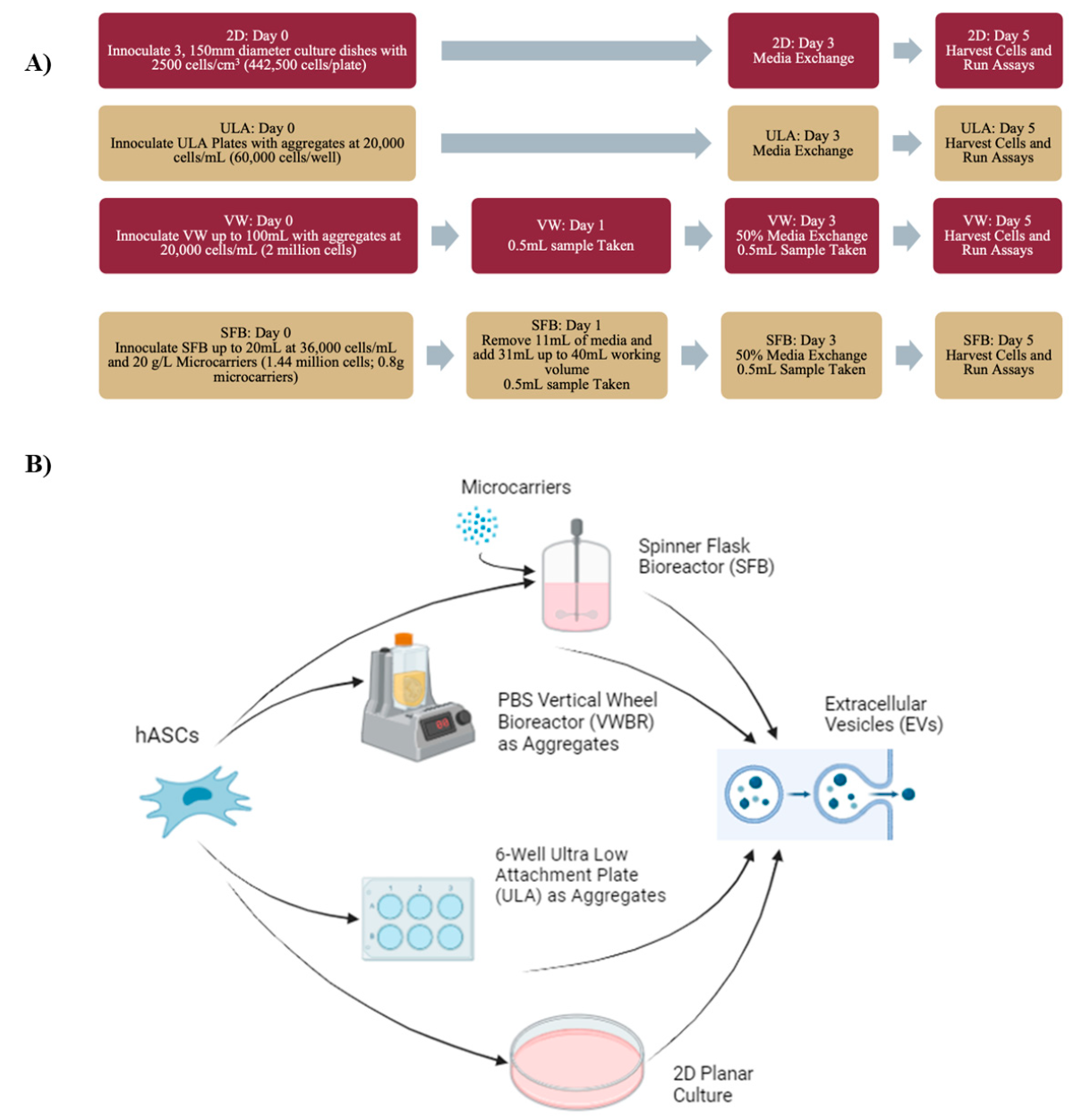
图4. 实验流程示意图。(A) 实验流程图,包含生物反应器设置、取样日期和实验概览。实验中用的Synthemax II 微载体。具体接种细胞数、接种效率、接种密度可参考原文。 (B) 实验生物反应器、静态聚集体对照组和二维对照组示意图。图中展示了hMSC的接种过程及收集的EVs。
之后研究团队做了三件关键的事:
收集各种培养方式下干细胞分泌的 “小包裹”- EVs,测一测产量(多少个)、大小,还有和 “小包裹生成” 相关的基因有没有更活跃;
测试这些 “小包裹” 的功能:比如能不能减少细胞的 “氧化应激”(相当于身体里的 “自由基伤害”)、能不能抑制炎症(比如减少导致炎症的 “坏因子” TNF-α);
模拟疾病场景测试:在类似阿尔茨海默病的模型里,看看 “小包裹” 能不能减少神经退化;还尝试把 “小包裹” 包在水凝胶里送进细胞,看看这种 “递送方式” 能不能提高抗炎效果。
2、关键结果:发现了啥有用的结论?
(1)动态生物反应器(尤其是 VWBR)比传统 2D 培养 “多产” 多了:
VWBR 产出的EVs 总量,比 2D 培养多了 1 倍多;比旋转瓶反应器也多出30%左右;
不管是每毫升培养基、还是平均每个干细胞产出的EVs都比 2D 培养多,而且相关的 “生成基因” 也更活跃(见原文)。
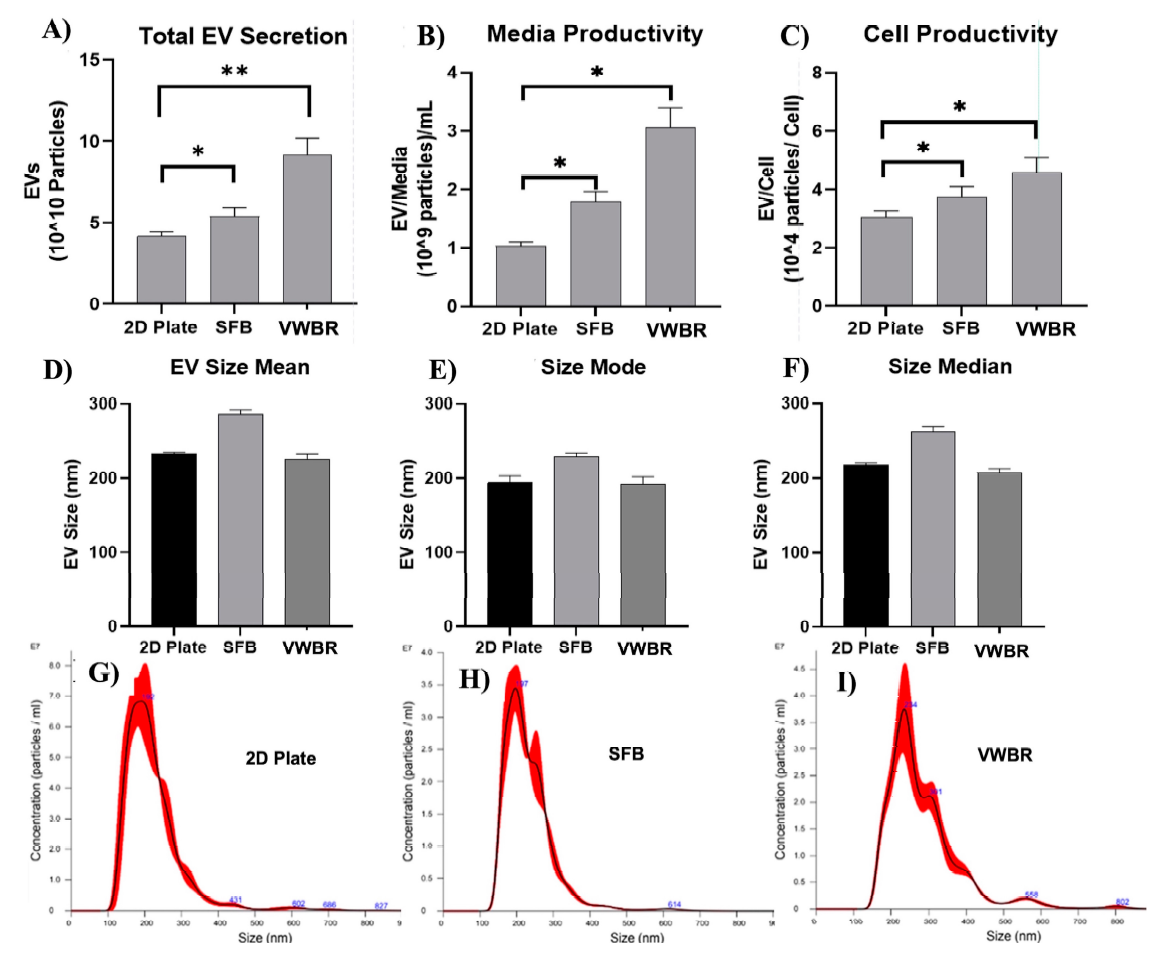
图5. 不同培养系统中细胞外囊泡的分泌情况,由纳米颗粒追踪分析(NTA)表征
(A) 从NTA计算得出的总EV产量。
(B) 按照培养基生产力归一化的EV产量(单位为每毫升培养基中的EV颗粒数)。结果显示,在SFB组中单位培养基生产力明显提高,几乎增加了2倍,而在VWBR组中则增加了3倍。
(C) 按照细胞生产力归一化的EV产量(单位为接种时D0的细胞计数下的EV颗粒数)。N = 3;* p < 0.05,** p < 0.01。EV的尺寸以均值 + 标准差表示。
EV尺寸分布图:(D) 平均尺寸;(E) 众数尺寸;(F) 中位尺寸。(G) 2D样本;(H) SFB;(I) VWBR。
(2)“小包裹” EVs的体外功能分析:
能明显减少 “氧化应激” 和炎症,比如在模拟阿尔茨海默病的模型里,能降低炎症因子,还能减少神经退化的标志;

图6. 在Aβ42寡聚体或阿尔茨海默病(AD)类器官培养基处理下,hMSC EVs的体外功能性实验。
(A) 电子传输显微镜(TEM)图像显示EVs。尺度条:60 nm。
(B) 四种不同EV样本的外泌体标志物Western blot分析。
(C) TNF-α分泌的ELISA分析。(I) Aβ42寡聚体增加了hMSC的TNF-α分泌;(II) EV处理Aβ42寡聚体刺激的细胞;
(D) 暴露于APOE4阿尔茨海默病(AD)相关脑类器官培养基的iPSC来源的围绕细胞(iPCs)。评估了hMSC EV处理对反应性氧种(ROS)生成的影响。(I) ROS定量;(II) ROS图像。尺度条:50 μm。*p < 0.05;*** p < 0.001。
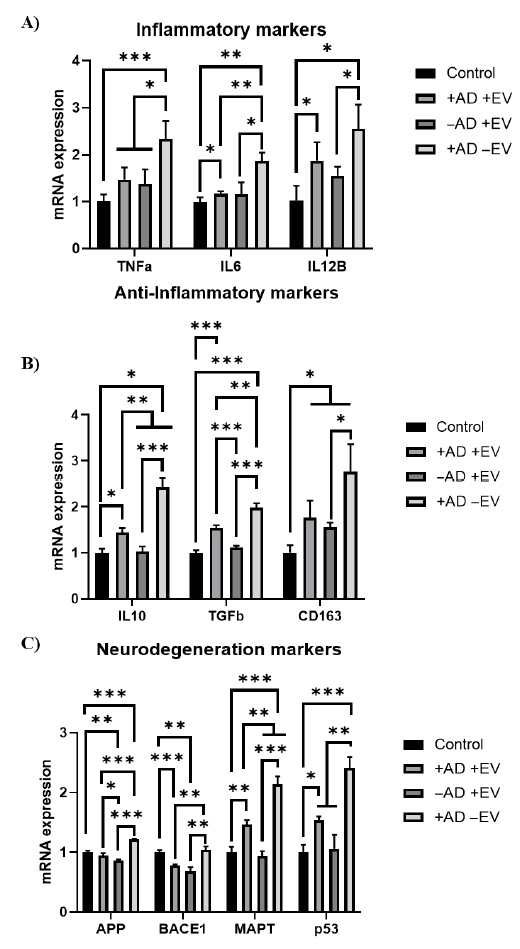
图7. 在阿尔茨海默病(AD)类脑器官培养基处理下,hMSC EVs对iPCs神经炎症和神经退行性标志物表达的影响。基因表达通过RT-qPCR进行测定。
(A) 炎症标志物;(B) 抗炎标志物;(C) 神经退行性标志物。N = 3。p < 0.05;** p < 0.01;*** p < 0.001,与对照组(无AD培养基和无EVs)比较。
把“小包裹”包在水凝胶里递送,抗炎效果更好(能阻止炎症相关的 NF-κB 信号激活)。(数据可见原文章)
三、总结
hMSCs 及其分泌的 EVs 因具有免疫调节和组织修复潜能,在退行性、炎症性疾病治疗中备受关注,但传统 2D 培养的 EVs 产量低,难以满足临床需求。文中分享的研究探究了在不同培养体系(尤其是可扩展生物反应器)对脂肪来源 hMSCs 分泌 EVs 的影响,同时验证 EV 的生物学功能,为 hMSC-EVs 的大规模生产和临床应用提供依据。提示生物反应器微环境(如流体动力学、剪切应力)可能通过调控 EVs 生物合成基因表达影响 EVs 产量,为进一步优化培养体系提供了理论基础。
参考资料
原文章DOI: 10.3390/bioengineering12090933(链接:https://doi.org/10.3390/bioengineering12090933)


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 













