
 发布时间:2025/11/25 点击数:787
发布时间:2025/11/25 点击数:787 体外寡核苷酸递送检测方法,用于评估靶向人肝细胞摄取及基因敲低效率
一、寡核苷酸具有独特的ADME/DMPK挑战,需要以人为本的方法
寡核苷酸疗法的兴起为复杂肝病治疗开辟了新的途径,为传统疗法难以奏效的疾病提供了靶向有效的解决方案。然而,由于核酸碱基序列与人类高度保守,寡核苷酸药物的研发面临着独特的体内挑战。
CN Bio的解决方案
PhysioMimix寡核苷酸递送分析利用体外人肝脏芯片,使您能够在与人类相关的模型中评估短寡核苷酸序列向肝脏的靶向递送、其被肝细胞吸收以及基因敲低效果。
寡核苷酸递送检测采用原代人肝细胞 (PHH),在灌注条件下进行3D培养,形成至少能保持14天功能的肝组织。与静态培养相比,灌注培养具有更高的生理相关性和更长的存活时间,使得通过单次或重复给药肝微组织,测量寡核苷酸的摄取和基因敲低效率,可以更准确地评估基于寡核苷酸的疗法的浓度效应。
该检测方法与以下方法兼容:
多种基于寡核苷酸的疗法,包括反义寡核苷酸(ASO)和小干扰RNA(siRNA)。
N-乙酰半乳糖胺(GalNAc)偶联物等递送系统能够将药物靶向输送到肝脏,从而治疗肝脏疾病。
此外,可通过临床可转化的生物标志物分析,在整个实验过程中监测芯片肝脏培养物的健康状况,从而识别潜在的不良反应。PhysioMimix DILI检测和试剂盒可提供更全面的毒性探索,包括肝脏固有免疫反应的激活。
二、CN Bio器官芯片的解决方案会带来什么好处?
1、克服发展挑战
PhysioMimix寡核苷酸递送检测提供了一种经济有效、符合伦理且与人类相关的方法,可以克服动物模型的物种间局限性,并加速基于寡核苷酸的治疗开发。
2、为诊所做好更充分的准备
利用该检测方法提供数据丰富的见解,证明进入人体研究的合理性,并通过评估给药策略为 I 期临床试验设计提供信息。
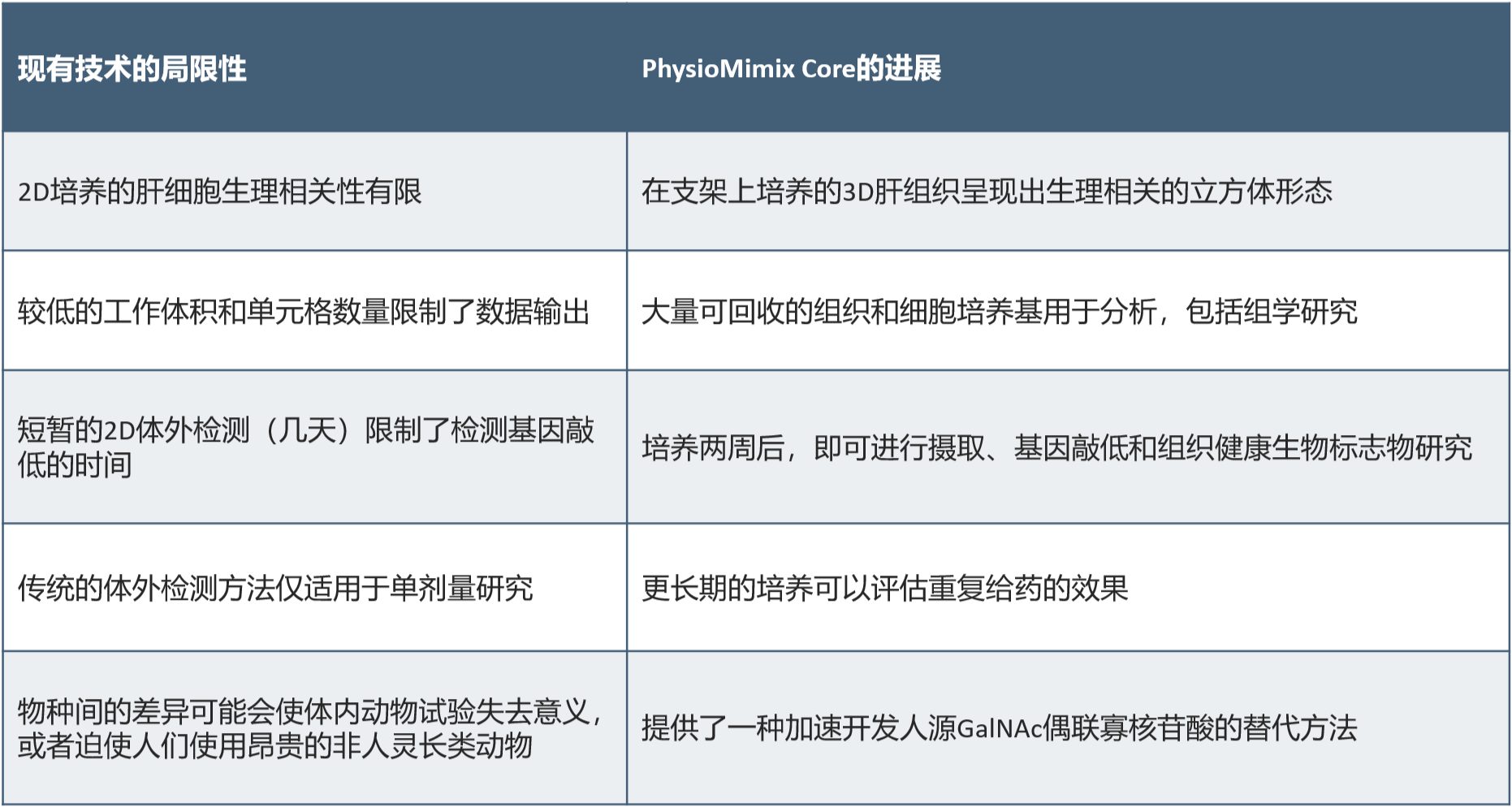
表:寡核苷酸递送的研究技术比较
三、使用CN Bio器官芯片研究标准寡核苷酸递送的检测时间表、检测终点
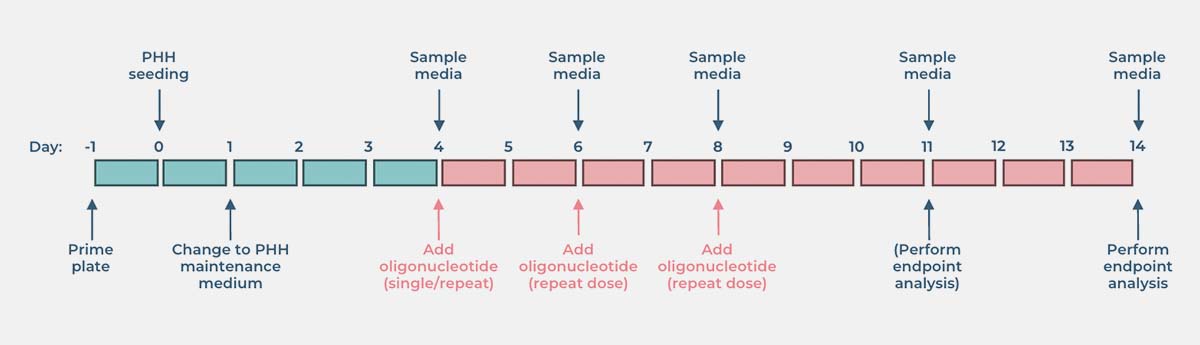
检测终点包括但不限于:
肝脏健康生物标志物:乳酸脱氢酶(LDH)、白蛋白、丙氨酸氨基转移酶/天冬氨酸氨基转移酶(ALT/AST)
寡核苷酸摄取:免疫荧光成像
基因敲除:qPCR、批量RNA测序
四、好处何以见得?
1、增强生理相关性
通过复制肝脏功能的关键方面,该检测方法缩小了体外检测与体内人类肝脏之间的差距。
Majer 等人(2024)[1]发表的一项研究表明,与生理相关性较低的圆形肝细胞相比,立方体状的原代人肝细胞在化学成分、形态和ASO分布方面存在差异。这使得人们对2D肝细胞检测方法(其中圆形肝细胞更为常见)在此目的上的适用性产生了质疑。

2、更深入的见解
PhysioMimix寡核苷酸检测的持久性使其能够同时评估寡核苷酸的吸收、基因敲低和组织健康状况。
评估GalNAc偶联siRNA和ASO与非偶联同类药物效果的研究表明,随着时间的推移,非GalNAc偶联ASO的肝细胞摄取(信号强度)高于GalNAc偶联ASO,这可能是由于ASO的加工方式不同所致。然而,基因敲低数据却呈现出不同的结果,凸显了同时测量这两个参数的重要性。 更多数据请查看CN Bio的点播网络研讨会[2]。
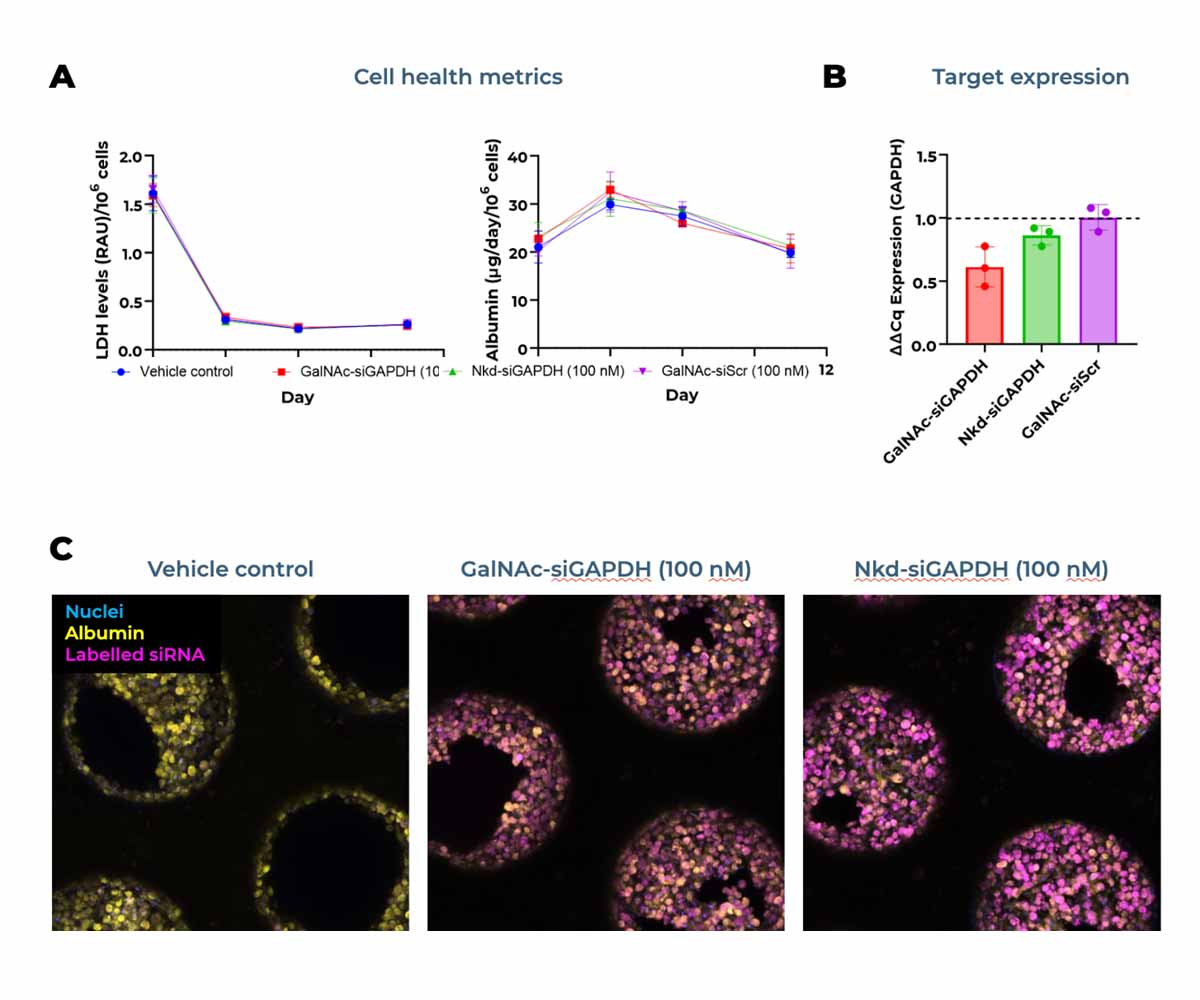
3、更完善的体内研究设计
14天的培养可以评估重复寡核苷酸治疗剂量的效果,从而为体内动物或first-in-human研究制定更合适的策略。
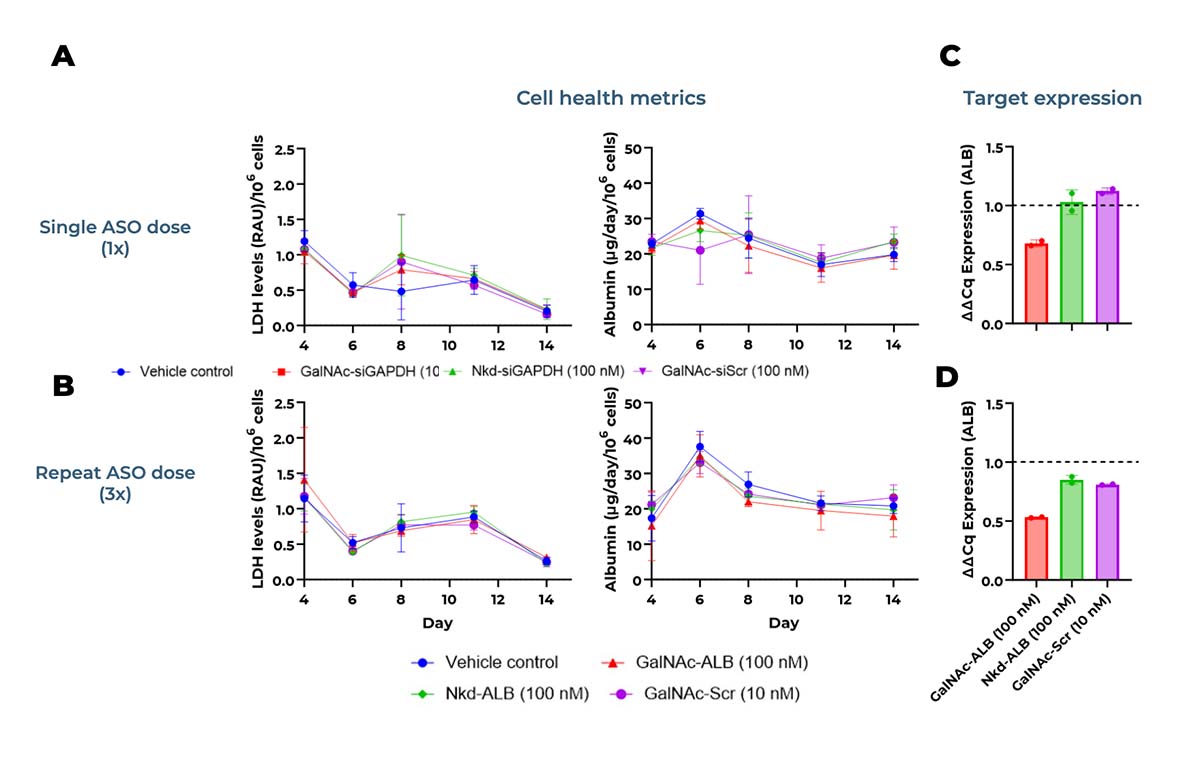
五、常见问题解答
(如果您的问题未在列表中找到答案,请联系我们)
Q1:我如何在我的实验室中重现PhysioMimix寡核苷酸递送检测?
要在您的实验室中复现PhysioMimix寡核苷酸摄取检测,您需要PhysioMimix 系统、我们3D验证细胞目录中的原代人肝细胞以及 Multi-chip Liver-12(货号:MPS-LC12) 芯片。请联系曼博生物获取实验方案指导。
Q2:你们的PhysioMimix寡核苷酸递送检测的通量是多少?
一台PhysioMimix控制器单元可以同时运行多达六块 MPS-LC12板,每次运行mostly可提供72个样本。
Q3:如何在PhysioMimix寡核苷酸递送分析中加入对照?
在我们的实验中,我们评估了针对目标序列的荧光标记非偶联寡核苷酸和 GalNAc 偶联寡核苷酸的特性,以及等效的对照寡核苷酸。这些对照共同构成了充分的实验对照,用于评估寡核苷酸摄取速率和数量的差异,以及基因敲低的具体效应。
Q4:如何使用PhysioMimix寡核苷酸递送检测方法在14天的实验窗口期内测量可溶性生物标志物?
PhysioMimix系统是一种组织培养装置,可利用原代细胞重建并维持人肝脏微组织。通过对培养基进行取样,可在多个时间点测量可溶性生物标志物。我们建议在每次更换培养基时采集培养基样本,即从寡核苷酸给药前第四天开始,每2-3天采集一次。
请查看上方的实验时间线以获得更直观的展示,简而言之,可以在第 6、8、11 和 14 天采集更多样本进行分析。每次更换培养基时,可采集 1.6 mL 培养基并冷冻保存以备分析。
Q5:在PhysioMimix寡核苷酸递送试验中,如何量化寡核苷酸的摄取量?
为了测量寡核苷酸的摄取,可在设定的时间点(测量摄取随时间的变化)从 Multi-chip Liver-12 芯片中取出肝脏微组织,时间范围为 4 至 14 天。取出的微组织在进行免疫荧光成像前需进行固定。请注意,如果需要进行纵向分析,建议每个时间点使用一块 Multi-chip Liver-12 芯片。
Q6:如何量化PhysioMimix寡核苷酸递送分析中的基因敲低?
为了测量寡核苷酸的摄取,可在设定的时间点(测量摄取随时间的变化)从 Multi-chip Liver-12 芯片中取出肝脏微组织,时间范围为 4 至 14 天。取出的微组织在进行免疫荧光成像前需进行固定。请注意,如果需要进行纵向分析,建议每个时间点使用一块 Multi-chip Liver-12 芯片。
Q7:我可以在PhysioMimix寡核苷酸递送试验中加入其他肝细胞类型,以评估肝细胞的特异性摄取吗?
目前,CN Bio的PhysioMimix寡核苷酸递送检测方法已在原代肝细胞单培养模型中得到验证。然而,Majer 等人(2024)[3]发表的一项研究探讨了该检测方法在利用库普弗(Kupffer)细胞共培养模型表征 ASO 递送和摄取至原代人肝细胞方面的应用,该模型使用多模态成像技术评估基于寡核苷酸的治疗吸收情况。此外,Rao S等人(2021)[4]利用三重培养肝病模型研究了 siRNA (siSPTBN1) 基因敲低的表型效应。
Q8:在PhysioMimix寡核苷酸递送试验中,我可以使用其他递送系统,例如脂质纳米颗粒吗?
CN Bio尚未验证脂质纳米颗粒(LNP)的使用,但是,没有明显的理由说明该方法不适合作为GalNAc偶联的替代方案。
Q9:您能否利用疾病模型研究寡核苷酸的摄取和基因敲低?
理论上来说,是的。我们之前已经探索过寡核苷酸疗法在我们为客户进行的代谢功能障碍相关性脂肪性肝炎(MASH,以前称为非酒精性脂肪性肝炎)检测中的疗效[5]。肝脏疾病模型,例如 PhysioMimix 代谢功能障碍相关脂肪变性 (MASH) 检测和NASH-in-a-box 试剂盒,均采用三培养(原代肝细胞、库普弗细胞和星状细胞)的芯片肝脏模型。这种方法为研究寡核苷酸疗效提供了一种替代途径,正如乔治·华盛顿大学的Rao S等人(2021)[4]在一项已发表的 siRNA 研究中探讨的那样,该研究旨在评估治疗预防癌症发展的效果。
此外,美国FDA发布的《寡核苷酸疗法开发临床药理学考量行业指南》[6]草案文件指出,“当寡核苷酸疗法靶向肝脏时,即药理靶点位于肝脏或存在针对肝脏的主动靶向作用时,申办方应考虑评估肝功能损害对耐受性、安全性和药效学的影响”。先前使用体外MASH模型可以为更好地指导研究设计提供初步见解。
Q10:我们能否利用PhysioMimix寡核苷酸递送检测来测试其他治疗方法?
在基于寡核苷酸的治疗药物类别中,我们已经测试了siRNA和ASO。预计该方法与其他寡核苷酸药物家族成员(例如microRNA(miRNA)和适配体)兼容。
更广地说,我们的芯片肝脏模型已被用于抗体检测,并且其用途已通过小分子得到了充足的验证。
拓展阅读
• CN Bio:一家经美国FDA验证过的微流控器官芯片系统供应商
参考链接
[1]https://pubs.rsc.org/en/content/articlelanding/2024/lc/d4lc00504j
[3]https://pubs.rsc.org/en/content/articlelanding/2024/lc/d4lc00504j
[4]https://pmc.ncbi.nlm.nih.gov/articles/PMC8941321/
[5]https://cn-bio.com/applications/disease-modeling/metabolic-dysfunction-associated-steatohepatitis/
[6]https://www.fda.gov/media/159414/download


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 













