
 发布时间:2026/04/15 点击数:262
发布时间:2026/04/15 点击数:262 Small重磅研究|PBS-Mini反应器3D培养体系赋能MSC-EVs角膜神经再生
视频
本文摘要
本文基于《Small》期刊发表的角膜神经再生前沿研究,系统解析了间充质干细胞来源细胞外囊泡(MSC-EVs)的制备关键参数,对比了2D常规培养与3D生物反应器培养体系对EVs产量、分子特征及角膜神经再生效能的影响,明确了组织来源与培养维度对EVs治疗效果的调控作用,为眼科再生医学领域的无细胞治疗研发提供了严谨的试验参考与数据支撑。

一、研究背景:角膜神经再生的临床困境与MSC-EVs的治疗潜力
角膜是人体神经支配很密集的组织,其感觉神经易受外伤、手术、疾病等因素损伤,而损伤后神经再生进程缓慢、常不完全,易引发角膜感觉减退、持续性上皮缺损、神经性疼痛等并发症,现有单因子治疗方案难以实现理想的解剖与功能恢复。
间充质干细胞(MSCs)来源的细胞外囊泡(EVs)作为新型无细胞治疗方案,是再生医学领域的研究热点。其可通过携带的蛋白、脂质、RNA等生物活性物质介导细胞间通讯,发挥抗炎、促再生等作用,为角膜神经损伤修复提供了新的解决思路。
本研究聚焦角膜来源MSCs(Co-MSCs)与骨髓来源MSCs(BM-MSCs)两大细胞来源,系统探究组织来源与培养维度对EVs角膜神经再生效能的影响,为EVs疗法的工艺优化与临床转化提供核心试验依据。
作为PBS Biotech、RoosterBio和Izon Science的官方合作伙伴,在外泌体研究领域,曼博生物可提供从上游细胞培养、EVs规模化制备,到下游分离纯化与表征的全流程物料与设备解决方案,包括本研究用到的RoosterBio专用培养基(点击查看https://www.mine-bio.com/roosterbio-msc-solutions-exosomes/)、PBS垂直轮生物反应器(点击查看https://www.mine-bio.com/PBS-Biotech/),助力国内外泌体相关研究与产业化落地。
二、研究设计:MSC-EVs制备与功能验证的全流程试验方案
Part1-该研究围绕MSC培养、EVs分离表征及功能验证展开了系统性试验设计,各环节关键参数与操作流程均明确量化,具体如下:
2.1 细胞来源与基础培养
选取5名不同供体的Co-MSCs与BM-MSCs,细胞均使用至第3-5代,保障实验用细胞的活性与均一性。细胞培养至80%-90%汇合度后,用于后续2D、3D培养体系的接种。
2.2 2D与3D培养体系构建
2.2.1 2D常规培养体系
采用T225培养瓶,以13000 cells/cm²的密度接种,培养至80%汇合度后,更换无血清培养基诱导EVs分泌,72小时后收集细胞分泌组(secretome),用于后续EVs分离。
2.2.2 3D生物反应器培养体系
基于PBS垂直轮式生物反应器开展3D培养,核心操作流程如下:
1) PBS Mini 0.1L反应器内加入1.25g预孵育的低浓度SynthemaxII微载体,接种2×10⁶个细胞,搭配90mL生长培养基(RoosterBasal MSC-CC培养基+2%的RoosterBooster-MSC-XF);
2) 先静置培养30分钟(20分钟后轻摇重悬未贴壁细胞,再静置10分钟),随后以25 rpm转速培养73小时;
3) 第3天取样计数细胞,并补加专用补充剂(RoosterBooster-MSC-XF),将转速调整至35 rpm继续培养;
4) 第5天更换无血清外泌体收集培养基(phenol red-free RoosterCollect-EV media),培养72小时后收集分泌组,经100μm细胞筛去除微载体后备用。

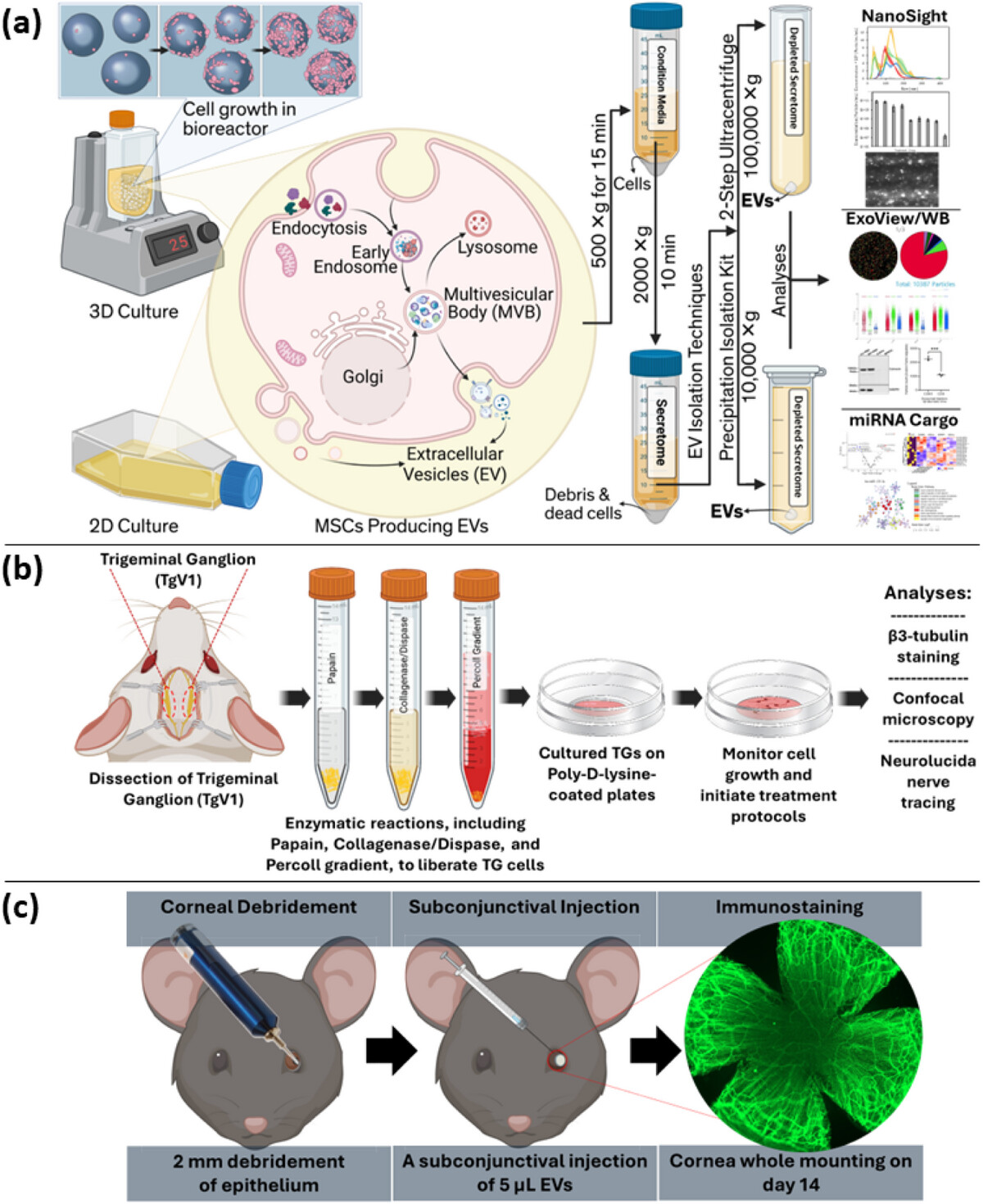
图1. MSC-EVs角膜神经再生研究实验流程示意图。
a)2D/3D体系扩增角膜/骨髓来源MSCs,完成EVs提取与多维度表征;
b)体外验证EVs对TgV1神经元神经突生长的促进作用;
c)体内验证EVs在角膜损伤模型中的神经再生修复效能。
2.3 EVs的分离与全面表征
两组培养体系的分泌组均先经梯度离心预处理,500×g离心15分钟去除细胞,2000×g离心10分钟去除细胞碎片;随后分别采用超速离心法和商业化沉淀试剂盒两种方法分离EVs,为保证EVs完整性,后续实验选用商业化试剂盒分离的产物。
表征环节通过多维度检测完成,核心检测项目包括:
• 纳米颗粒跟踪分析(NTA)检测EVs的颗粒浓度与尺寸分布;
• ExoView分析CD9、CD81、CD63等四跨膜蛋白表达特征;
• 蛋白质印迹法(Westernblot)验证外泌体标志物ALIX、细胞污染标志物Calnexin等蛋白表达,确认EVs纯度;
• 透射电子显微镜(TEM):观察EVs的形态特征。
2.4 EVs神经再生功能验证
2.4.1 体外功能验证
分离4-6周龄小鼠三叉神经节神经元(TgV1),接种于多聚赖氨酸包被的培养皿,待出现初始神经突生长后,加入不同组别EVs(终浓度2×10⁹个/培养皿),培养48小时后,通过βIIItubulin免疫荧光染色,结合Neurolucida软件定量分析神经突长度,并通过GAP-43染色检测神经再生芽生情况。
2.4.2 体内功能验证
构建10-12周龄小鼠2mm角膜上皮清创损伤模型,对损伤眼结膜下注射5μL EVs(含2×10⁹个颗粒),设置空白培养基组为对照;术后14天解剖小鼠角膜,经免疫荧光染色后,量化角膜中心1mm区域的神经长度;同时采用vonFrey细丝检测角膜眨眼阈值,评估角膜感觉神经的功能恢复情况。
2.5 分子机制探究
对不同培养体系、不同组织来源的EVs进行小RNA测序,分析其miRNA表达谱,筛选差异表达miRNA;通过RT-qPCR验证关键miRNA的表达水平,并结合靶基因预测与通路富集分析,探究EVs调控角膜神经再生的分子机制;同时检测TgV1神经元中神经再生相关基因的表达,验证通路调控作用。
三、核心结果:3D培养体系对MSC-EVs产量与再生效能的关键影响
Part2-该研究通过多维度检测,客观呈现了PBS反应器3D培养体系在MSC-EVs制备中的表现与优势,核心试验结果均以定量数据呈现,具体如下:
3.1 3D培养提升MSC-EVs的产量与优质颗粒占比
NTA检测结果显示,3D培养体系的EVs颗粒浓度明显高于2D培养,核心数据如下:
• 3D-BM-MSC-EVs颗粒浓度:(1.03±2.72)×10¹¹个/mL
• 3D-Co-MSC-EVs颗粒浓度:(8.64±1.96)×10¹⁰个/mL
• 2D-BM-MSC-EVs颗粒浓度:(5.37±1.35)×10⁹个/mL
• 2D-Co-MSC-EVs颗粒浓度:(1.41±1.32)×10¹⁰个/mL
两组数据差异具有统计学意义(p<0.05)。
粒径分布分析显示,所有组别EVs中80%以上颗粒直径小于200nm,符合外泌体典型尺寸范围;其中3D培养组的小尺寸颗粒占比更高,3D-BM-MSC-EVs为88.3%±4% ,3D-Co-MSC-EVs为91.0%±2%。

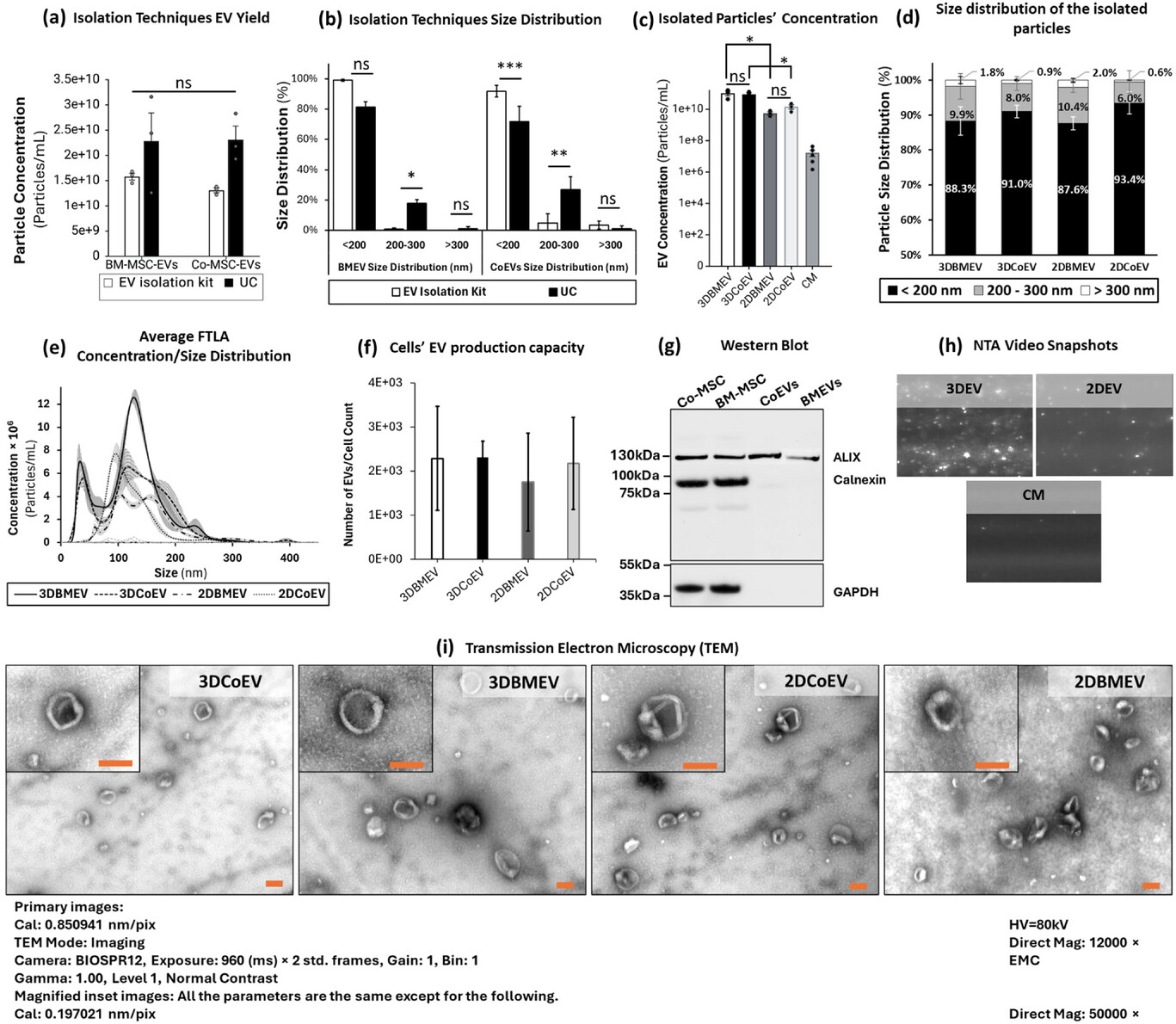
图2. MSC-EVs的分离方法对比与多维度表征结果。
a)分离方法对比:超速离心法(UC)获得的EVs产量更高,但与商业化沉淀试剂盒相比,差异无统计学意义;
b)小尺寸EVs富集效果:商业化试剂盒分离的<200nm小尺寸EV占比更高,其中角膜来源EVs(CoEVs)组差异具有统计学意义,骨髓来源EVs(BMEVs)组无明显差异;
c)培养维度对产量的影响:纳米颗粒跟踪分析(NTA)显示,3D培养来源EVs的颗粒浓度高于2D培养组(p<0.05),证实3D培养可提高EVs产量;
d)粒径分布特征:四个EVs实验组中,超80%的颗粒直径小于200nm,符合外泌体的典型尺寸范围;
e)FTLA分析:所有EVs样本的浓度/粒径分布趋势一致,峰值均低于200nm;
f)各组间单位细胞产生的EVs数量无明显差异,实验分组间具备可比性;
g)EVs纯度验证:Western blot结果显示,EVs组分富集外泌体标志物ALIX,未检出细胞污染标志物Calnexin与GAPDH,而母细胞裂解液中可检出上述三种蛋白,证实EVs纯度达标;
h)NTA可视化结果:3D培养来源EVs的颗粒浓度高于2D组,空白收集培养基(CM)中仅检出少量颗粒;
i)形态学验证:所有EVs组的透射电子显微镜(TEM)图像证实,存在具有外泌体典型杯状和球形形态的纳米颗粒。
注:图中误差线代表标准误(SE);星号表示差异具有统计学意义;每组设3个生物学重复;比例尺=200nm。
3.2 3D来源EVs体外促神经再生效果优于2D组
体外实验结果证实,3D培养体系来源的EVs促进TgV1神经元神经突生长的效果更明显
3D-Co-MSC-EVs处理组神经突长度为12.64±1.5mm,3D-BM-MSC-EVs处理组为10.21±1.24mm,均明显高于对应的2D培养组(2D-Co-MSC-EVs组5.3±0.58mm、2D-BM-MSC-EVs组3.0±0.32mm),且p<0.05;同时3D-EVs处理组的GAP-43阳性信号更强,神经再生芽生更活跃。

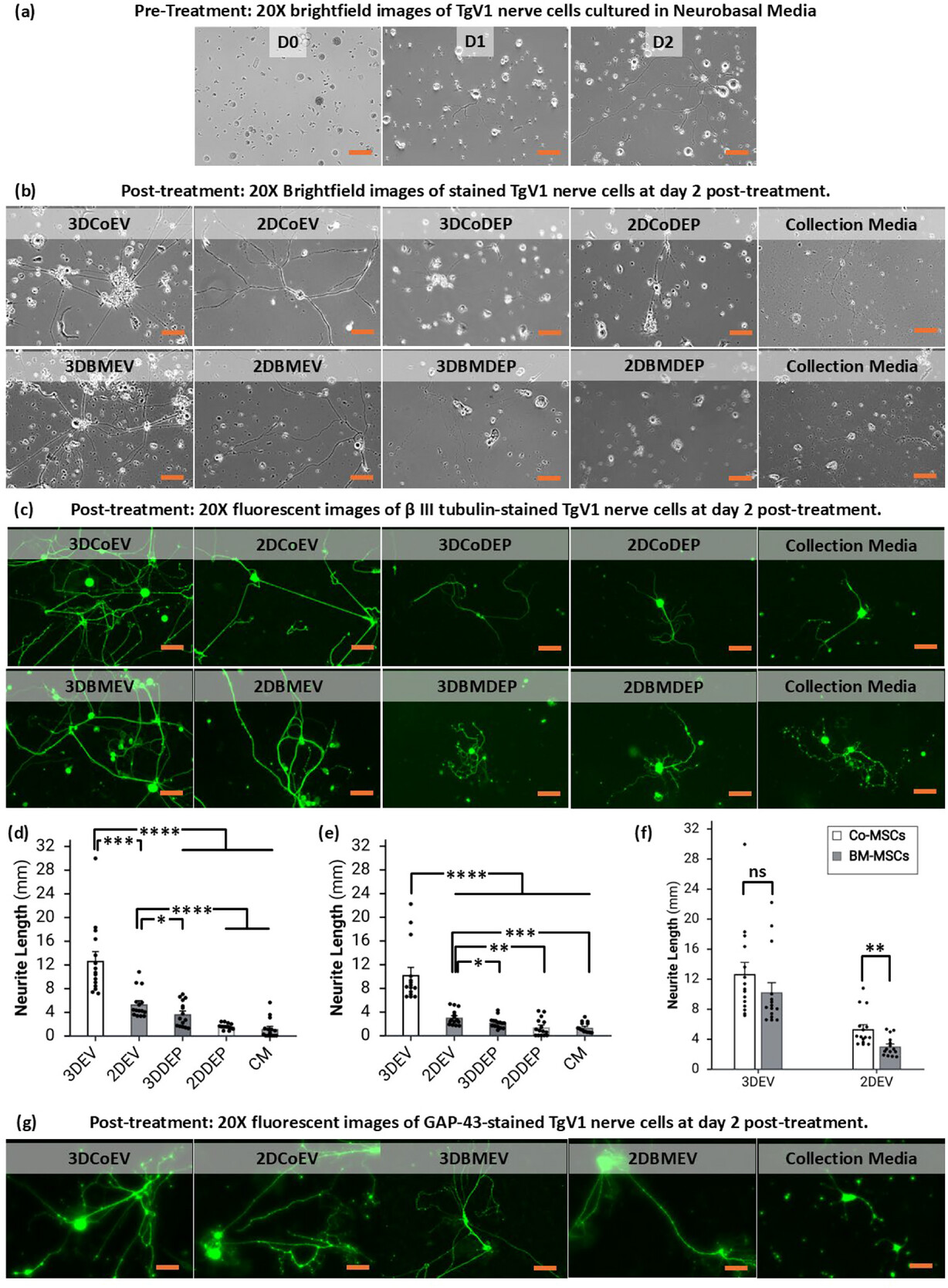
图3. MSC-EVs对三叉神经节神经元神经突生长的体外功能验证。
a)明场图像展示了处理前(培养至第2天)的神经突生长状态;
b)处理48小时后的20倍明场图像显示,3D培养来源EVs处理组的神经元神经突生长,优于2D培养来源EVs处理组及各对照组;
c)β-Ⅲ微管蛋白荧光成像进一步证实,3DEV处理组的神经生长情况优于2DEV组与空白对照组;
d-f)Neurolucida定量分析结果显示,无论是角膜来源(CoEVs)还是骨髓来源(BMEVs)的EVs,3DEV处理组的神经突伸长量均高于对应的2DEV处理组;
g)GAP-43免疫荧光成像显示,3DEV处理组的神经再生相关信号强于2DEV处理组与空白培养基(CM)对照组。
3.3 3D来源EVs体内角膜神经修复与功能恢复效果更突出
术后14天,3D-EVs处理组小鼠角膜神经再生与功能恢复均优于2D组及空白对照组,3D-Co-MSC-EVs组角膜神经长度为51.9±9.1mm,3D-BM-MSC-EVs组为42.2±3.5mm,高于对照组的23.3±1.2mm(p<0.01);角膜敏感性检测中,3D-EVs处理组的眨眼阈值明显低于对照组,表明感觉神经功能恢复更理想。

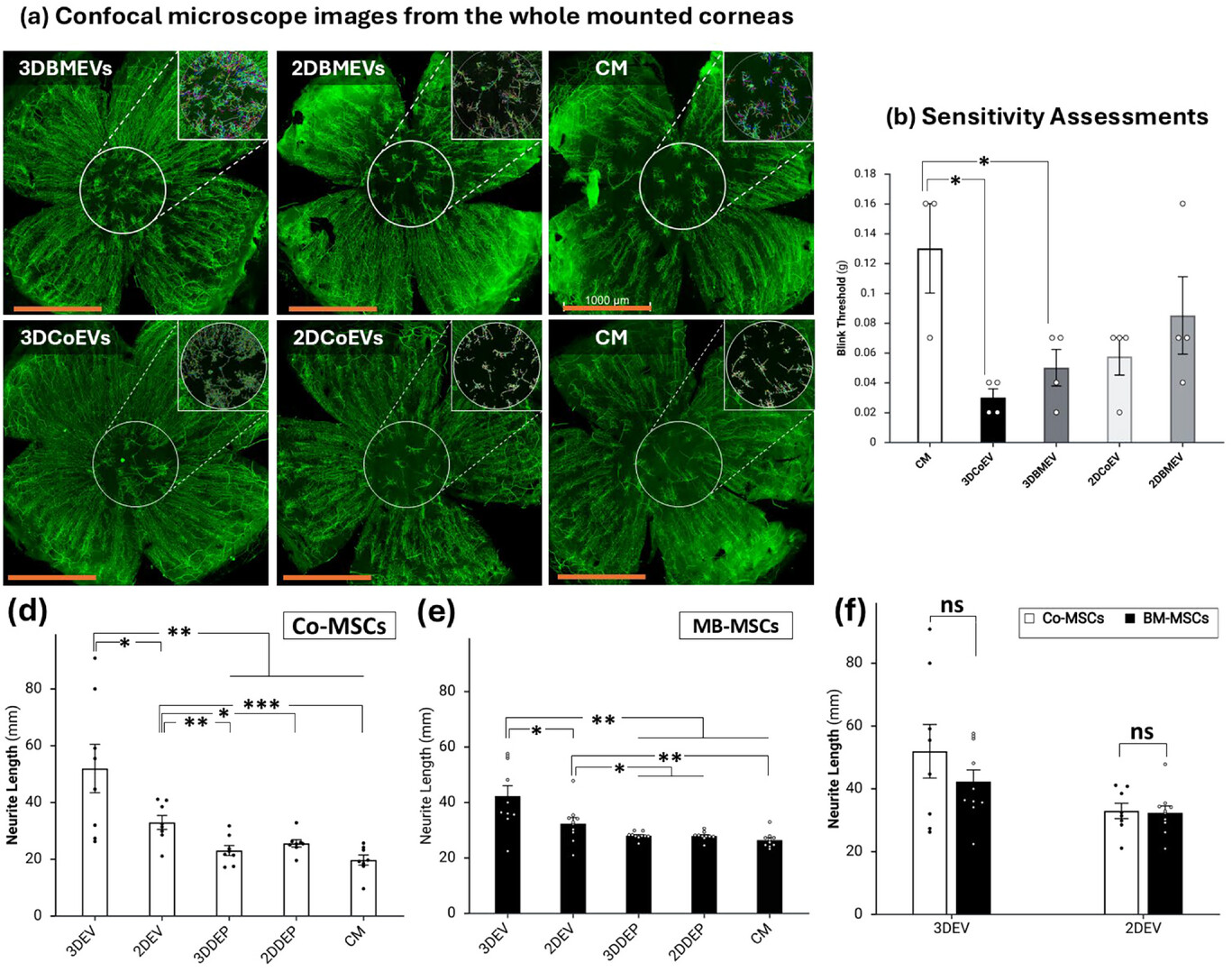
图4. MSC-EVs在小鼠角膜损伤模型中的体内神经再生与功能恢复效果验证,角膜清创及治疗注射后2周,通过βIIITubulin抗体染色结合Neurolucida分析评估神经再生情况
a)对角膜中央1mm区域的神经纤维密度进行定量分析;(a插图)小图为再生神经的代表性追踪结果,采用NeurolucidaExplorer软件进行彩色标记和测量。
b)与2DCoEV)处理组及对照组相比,3DCoEVs处理组的角膜神经生长增加,差异具有统计学意义。
c)与2DBMEVs处理组及对照组相比,3DBMEVs处理组的角膜神经生长明显增加,差异具有统计学意义。
d)CoEVs处理组的角膜神经再生效果略优于BMEVs处理组,但差异无统计学意义。
e)采用冯・弗雷细丝(vonFreyhairfilaments)评估角膜神经功能:眨眼阈值越高表明敏感性越低;对照组角膜的眨眼阈值高,而3DCoEVs处理组的角膜敏感性好;所有EVs处理组的角膜敏感性均优于对照组。采用双尾独立样本t检验评估不同处理对损伤角膜神经再生的统计学影响;比例尺=1000μm;每组条件设4个生物学重复;CM代表未处理收集培养基。
3.4 培养维度改变EVs的miRNA表达谱
小RNA测序显示,3D培养明显改变了EVs的miRNA表达谱,3D-BM-MSC-EVs中hsa-miR-128-3p、hsa-miR-409-3p等神经营养相关miRNA高表达,3D-Co-MSC-EVs中则富集调控细胞外基质重塑的miRNA;且3D培养降低了不同组织来源EVs的miRNA表达异质性。RT-qPCR验证显示,3D-EVs处理能明显上调TgV1神经元中神经突生长、突触形成及基质重塑相关基因的表达。

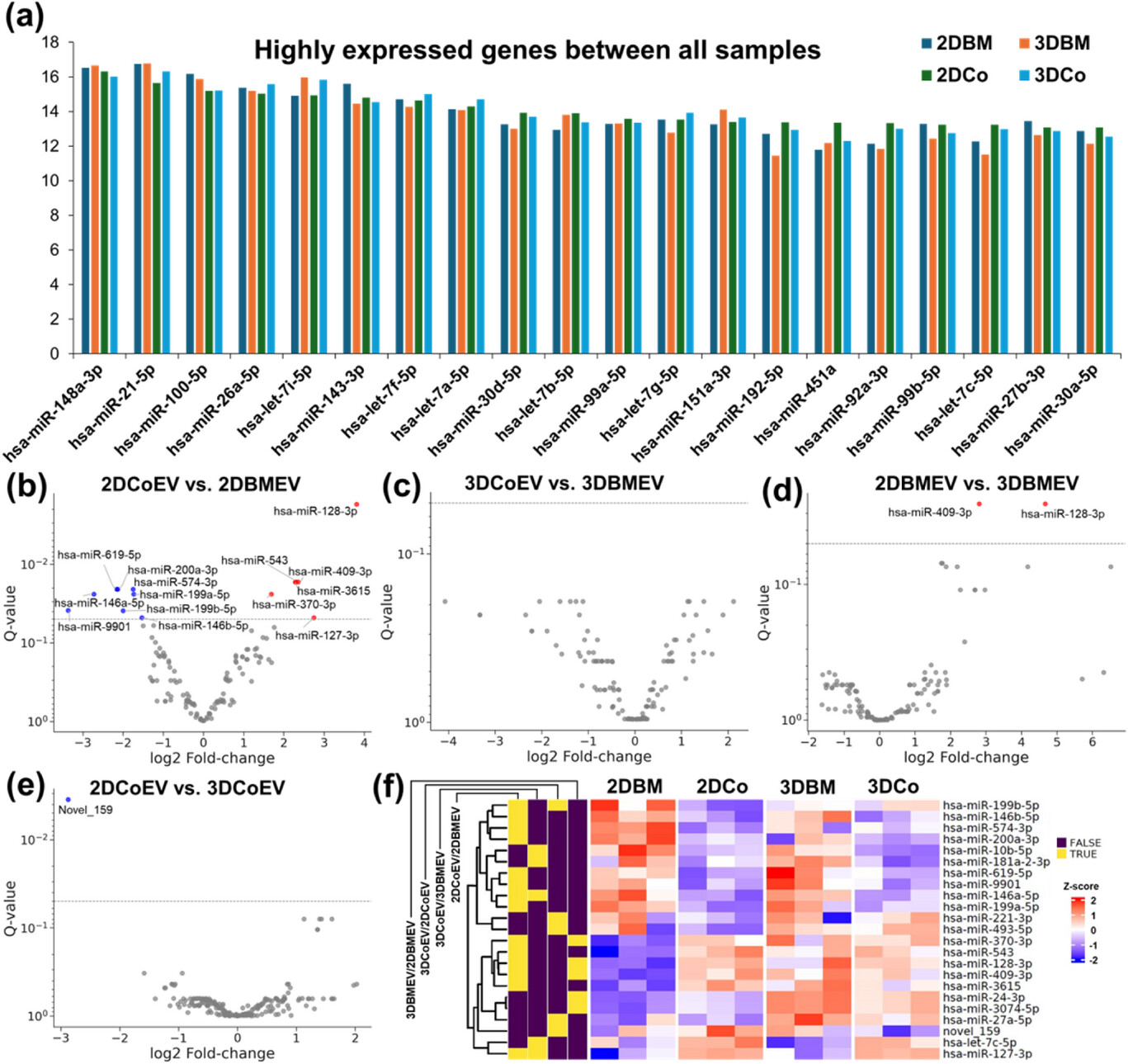
图5. 不同组织来源及培养条件下MSC-EVs的miRNA表达谱特征。
a)柱状图显示2D和3D培养的BM-MSC及Co-MSC来源EVs中,共有的20种高丰度表达miRNA。
b)2D CoEVs与2D BMEVs的对比分析显示,差异表达的miRNA数量多,表明二维培养条件下不同组织来源EVs的分子差异明显。
c)3D CoEVs与3D BMEVs的对比分析显示,差异表达miRNA数量大幅减少,表明三维培养条件下不同组织来源EVs的分子相似性更高。
d)3D BMEVs与2D BMEVs的对比分析显示,部分miRNA明显上调,表明培养维度对BMEVs的内容物组成影响突出。
e)相反,3D CoEVs与2D CoEVs的对比分析仅发现1种miRNA(hsa-miR-159)表达明显改变,表明角膜间充质干细胞来源EVs的内容物组成在不同培养维度下相对稳定。
f)miRNA表达热图显示,样本按培养条件呈明显聚类,且3D培养组的组织特异性差异较2D培养组有所降低。
四、研究价值与产业转化意义
本研究通过严谨的试验设计,系统证实了PBS垂直轮式生物反应器的3D培养体系在MSC-EVs制备中的核心应用价值:其低剪切力的流体动力学设计构建的仿生微环境,既保证了细胞活性,又优化了EVs的产量与功能;同时明确了组织来源对EVs治疗效能的影响,为角膜神经再生的EVs疗法优化提供了直接的试验依据。值得注意的是,研究中细胞扩增与EVs收集全程采用RoosterBio专用培养基,其化学成分限定的无血清配方,为试验结果的可靠性与后续临床转化提供了保障。
曼博生物作为PBS Biotech、RoosterBio和IZON Science官方供应商,致力于将这类经过科研验证的优质生物工艺解决方案引入国内,为再生医学、细胞治疗领域的研究与产业化提供有力支持。
在外泌体研究领域,曼博生物可提供全流程上下游物料与设备解决方案,包括:
• RoosterBio系列产品(点击查看https://www.mine-bio.com/roosterbio-msc-solutions-exosomes/):MSC无血清培养基、EVs收集专用培养基等,助力CGT研发与规模化生产;
• PBS垂直轮生物反应器(点击查看https://www.mine-bio.com/PBS-Biotech/):覆盖从研发到规模化生产的全阶段3D悬浮培养需求;
• IZON品牌外泌体相关设备(点击查看https://www.mine-bio.com/izon-products/):提供外泌体分离、纯化和表征全流程解决方案。
拓展阅读
曼博生物官方代理RoosterBio|MSC及外泌体培养基赋能中国CGT研发与规模化生产:https://www.mine-bio.com/IndustryNews/roosterbio-news-01.shtml


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 















