
 发布时间:2026/05/06 点击数:10
发布时间:2026/05/06 点击数:10 用于研究基于寡核苷酸疗法的递送与疗效的肝脏微生理系统
(注:本文原英文资料可联系上海曼博生物获取)
本文核心信息
寡核苷酸疗法具有高度的人类特异性,需要更为以人为中心的开发方法。
微生理系统(MPS)以更具生理相关性的方式复制细胞和组织的结构和功能性生物标志物。
我们的研究证明了肝脏MPS和寡核苷酸递送测定在检测靶向肝脏的寡核苷酸的摄取和基因敲低方面的有效性。
MPS的洞察有助于推动那些动物模型适用性较差的新型模式药物的开发,从而使初次人体研究的信息更充分。
一、引言:寡核苷酸疗法临床前测试的核心痛点
随着新药物模式进入临床试验,对与人体相关的体外模型的需求日益增加。传统的临床前动物模型通常无法准确预测药物的疗效和毒性,导致后期药物损耗率居高不下。诸如寡核苷酸疗法等新药物模式具有高度的人体特异性,需要以人体为核心的开发方法。非人物种通常不适合进行测试,而更相关的选择,如非人灵长类动物,不仅成本高昂,而且在伦理上存在挑战。因此,与人体相关的新方法方法学,例如器官芯片技术,对于提高临床前测试的预测能力很重要。器官芯片,也称为微生理系统,通过在灌注式3D支架上培养原代人体细胞,以更具生理相关性的方式复制细胞和组织的功能性生物标志物(Rubianoetal.,2021)。在初次人体试验之前,MPS有潜力为评估和设计寡核苷酸疗法提供一种更具生理学意义的途径。
基于寡核苷酸的疗法,即基于RNA的疗法,是干扰特定RNA分子的短序列,包括反义寡核苷酸、RNA干扰、小干扰RNA、微小RNA和适配体(Robertsetal.,2020)。对这些疗法的兴趣源于对人类基因组的理解,以及相较于传统小分子化合物,它们更快的药物发现过程。更近的进展,如脂质纳米颗粒和GalNAc偶联技术,实现了向肝脏的靶向药物递送。GalNAc通过肝细胞上的去唾液酸糖蛋白受体靶向肝脏。GalNAc偶联的寡核苷酸与ASGPR结合,被内吞,并释放治疗性寡核苷酸以靶向特定的mRNA序列(Debackeretal.,2020)。该方法增强了效力,减少了脱靶效应,并允许更长的给药间隔和更低的免疫原性。因此,基于GalNAc的疗法在治疗遗传、代谢和感染性疾病方面具有巨大潜力。
由于寡核苷酸通过GalNAc相关的内吞作用被肝细胞快速摄取,该策略已被用于设计靶向肝脏疾病的疗法。它在治疗传统药物失败的"不可成药"疾病方面显示出前景。因此,我们选择在PhysioMimix肝脏MPS和寡核苷酸递送测定中,使用GalNAc偶联策略靶向原代人肝细胞,研究小干扰RNA和反义寡核苷酸。曼博生物官方供应CN Bio的PhysioMimix微流控芯片系统,可点击查看曼博生物提供的PhysioMimix微流控芯片系统详细信息(https://www.mine-bio.com/CN-Bio-Innovations/Physiomimix.shtml)。
二、研究目的:建立肝脏MPS寡核苷酸递送评价体系
我们介绍CNBioPhysioMimix肝脏MPS,用于研究寡核苷酸向肝脏的递送及其被原代人肝细胞的摄取。该肝脏MPS能生成功能稳定、状态良好的原代人肝细胞微组织,从而能够在14天内进行基因敲低和给药策略的研究。
为满足对此类疗法进行适当体外测试日益增长的需求,我们在寡核苷酸递送测定中,使用带有和不带GalNAc偶联的荧光标记小干扰RNA或反义寡核苷酸靶向原代人肝细胞。我们的结果显示,原代人肝细胞能有效摄取,并随后敲低目标基因。
三、实验材料与方法:肝脏MPS寡核苷酸递送与基因敲低评价体系
每项实验均使用PhysioMimix Core系统和定制的多芯片肝脏-12板进行。该板含有12个孔,每个孔内有独立的胶原蛋白涂层支架,原代人肝细胞以每支架0.6×10⁶个细胞的密度接种(图1A-B)。支架内的孔隙与灌注系统相结合,使细胞培养基能够流过所形成的肝脏微组织(图1C)。
使用靶向GAPDH基因的荧光标记GalNAc-小干扰RNA处理原代人肝细胞。这些包括:GalNAc-siGAPDH-Cy5;Naked-siGAPDH-Cy5;或GalNAc-siScrambled-FAM。除GalNAc-小干扰RNA外,我们还研究了靶向白蛋白基因的GalNAc-反义寡核苷酸。使用了以下反义寡核苷酸:GalNAc-ALBASO-Cy5;Naked-ALBASO-Cy5;或GalNAc-非靶向乱序反义寡核苷酸-FAM。使用共聚焦显微镜对支架进行Cy5或FAM标记成像;并分离RNA,使用qPCR技术测试GAPDH基因的敲低情况。我们研究了不同浓度(10nM-100nM)反义寡核苷酸的摄取和基因敲低效应,以及在基于肝脏MPS的寡核苷酸递送测定中,单次给药与重复给药的效应比较。
每2-3天进行一次培养基更换,并使用培养基样品评估细胞健康状况和损伤情况。通过分别使用显色法测定乳酸脱氢酶和酶联免疫吸附测定法定量白蛋白的产生,评估肝细胞的健康状况和功能性。通过免疫细胞化学评估摄取,实验结束时,使用一半支架,经4%多聚甲醛固定后,进行白蛋白以及Hoechst 33342染色。使用Zymo Research的RNA Shield和Quick-RNA Microprep试剂盒从剩余的一半支架中提取RNA。使用Invitrogen的高容量RNA-to-cDNA试剂盒,随后使用TaqMan Fast Advanced Master Mix和TaqMan基因表达测定进行qPCR,评估目标基因表达。目标基因表达以定量循环值表示,并使用内参基因Cq值进行归一化,显示为ΔΔCq表达,先归一化至培养基对照(Livak and Schmittgen, 2001)。
四、实验结果:PhysioMimix系统下寡核苷酸摄取与疗效评估
结果一:使用PhysioMimix Core微生理系统生成3D人肝脏微组织
我们使用带和不带GalNAc偶联的标记小干扰RNA和反义寡核苷酸,探索在基于PhysioMimix肝脏MPS的寡核苷酸递送测定中使用这些新药物模式。原代人肝细胞在第0天接种到各孔中,每2-3天更换培养基并取样,寡核苷酸在第4天添加一次,或在第4、6、8天添加三次,或用培养基对照处理(图1D)。在胶原蛋白涂层支架上可生成稳定且有功能的原代人肝细胞,用于评估标记寡核苷酸的摄取情况(图1E)。
图1.使用PhysioMimix核心微生理系统生成3D人肝脏微组织。(A)PhysioMimix概览,包括控制器、扩展坞和三个带有多芯片肝脏-12板的驱动器。(B)多芯片肝脏-12板示意图,显示一个开放式细胞培养孔的横截面,其中包含用于肝细胞生长的3D支架。(C)微泵驱动细胞培养基循环,促进营养物质和气体交换。每板可培养多达12个肝脏微组织。(D)在14天内对肝脏MPS进行寡核苷酸给药的时间线。(E)通过明场显微镜成像的支架上的3D人肝脏微组织。比例尺:200μm。
结果二:在肝脏MPS中引入GalNAc偶联、荧光标记的小干扰RNA
细胞损伤(乳酸脱氢酶)和细胞健康(白蛋白)的读数显示,所使用的小干扰RNA之间没有差异。所有实验中,乳酸脱氢酶水平通常起始于1.5-2.0RAU/10⁶个细胞左右,保持一致。该原代人肝细胞供体的白蛋白产量维持在20-40μg/天/10⁶个细胞之间,峰值产量通常出现在第6天(图2A)。使用GalNAc偶联的靶向小干扰RNA处理原代人肝细胞,观察到更大的目标基因(GAPDH)敲低效果(GalNAc-siGAPDH,图2B)。实验结束时,肝脏微组织仍保持功能性,通过阳性白蛋白染色显示,该染色同时也用于共标记原代人肝细胞(图2C)。
如图2C所示,确认了原代人肝细胞在支架孔隙中摄取了Cy5标记的小干扰RNA。尽管与GalNAc-siGAPDH图像相比,Nkd-siGAPDH图像中的信号强度更高(品红色,图2C),表明该模式摄取更多,但GalNAc偶联模式在基因表达水平上效果更大(图2B)。这种差异可能是由于小干扰RNA的摄取/内吞或加工方式不同所致。
图2.在肝脏MPS中引入GalNAc偶联、荧光标记的小干扰RNA。原代人肝细胞用浓度为0nM和100nM的小干扰RNA处理三次(第4、6、8天)。(A)在为期11天的实验中,观察到低乳酸脱氢酶和稳定的白蛋白产量,表明细胞健康。(B)与非偶联的小干扰RNA相比,GalNAc偶联的siGAPDH对目标(GAPDH)基因表达的敲低效果更大。(C)固定后的免疫荧光成像显示Cy5标记小干扰RNA的摄取(品红色);细胞核(蓝色)和白蛋白(黄色)。比例尺:50μm。
结果三:GalNAc偶联靶向小干扰RNA对GAPDH的剂量依赖性敲低
接下来,我们研究了GalNAc偶联的靶向小干扰RNA对GAPDH的敲低是否存在剂量依赖性。在原代人肝细胞第4、6、8天用浓度为10、50或100nM的小干扰RNA处理三次。如低乳酸脱氢酶水平和稳定的白蛋白产量所示,在为期11天的实验过程中,对细胞健康无不良影响(图3A)。我们观察到GalNAc-siGAPDH对GAPDH基因表达的敲低呈剂量依赖性,而在Nkd-siGAPDH条件下未观察到浓度效应(图3B)。同时观察到随着浓度增加,小干扰RNA的摄取增加(品红色,图3C)。
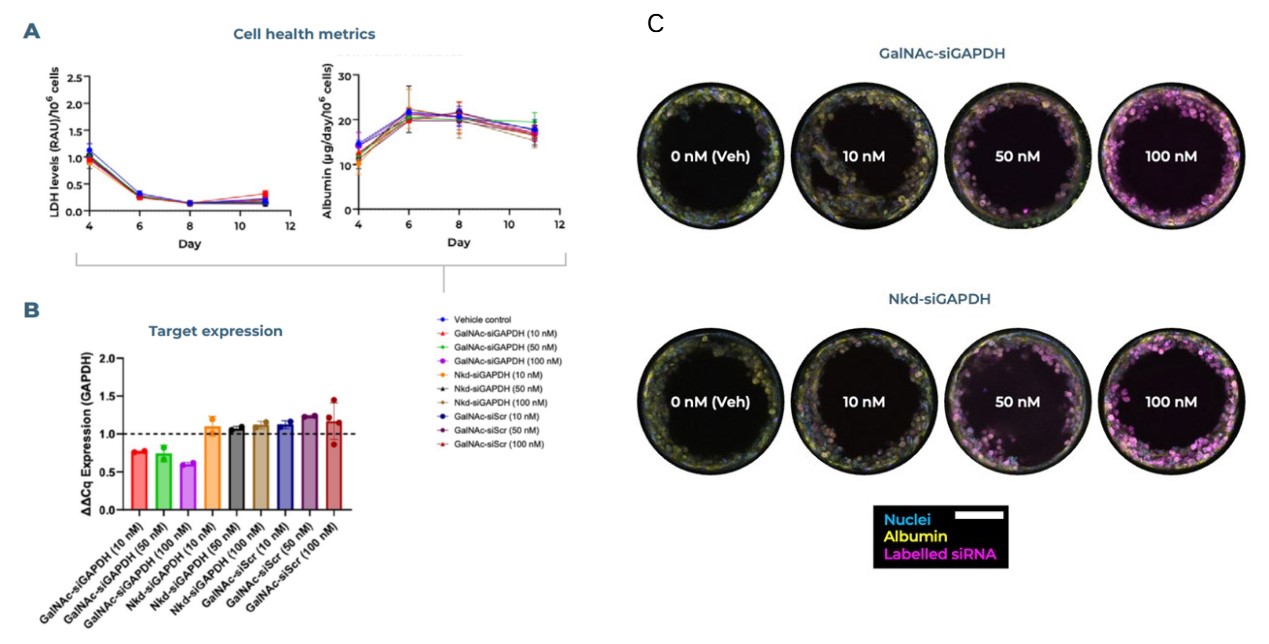
图3.GalNAc偶联靶向小干扰RNA对GAPDH的剂量依赖性敲低。原代人肝细胞用浓度为0、10、50和100nM的小干扰RNA处理三次(第4、6、8天)。(A)在为期11天的实验中,观察到低乳酸脱氢酶和稳定的白蛋白产量,表明细胞健康。(B)GalNAc-siGAPDH对目标(GAPDH)基因表达的敲低呈剂量依赖性;在Nkd-siGAPDH条件下未观察到增加浓度的效应。(C)固定后的免疫荧光成像显示Cy5标记小干扰RNA的摄取(品红色);细胞核(蓝色)和白蛋白(黄色)。比例尺:100μm。
结果四:单次给药下反义寡核苷酸的持续摄取和有效基因靶向
使用靶向白蛋白基因表达的反义寡核苷酸,我们先在14天周期内,于第4天对原代人肝细胞进行了一次处理。比较第14天标记反义寡核苷酸的摄取,与GalNAc-ALBASO相比,Nkd-ALBASO的信号更强(图4A)。尽管如此,我们观察到在GalNAc-ALBASO条件下对ALB基因表达的敲低更多(图4B),这与在GalNAc-小干扰RNA中观察到的结果一致(图2)。进一步的研究可以调查偶联与非偶联寡核苷酸在原代人肝细胞中的亚细胞定位,以更好地理解这些观察到的差异。
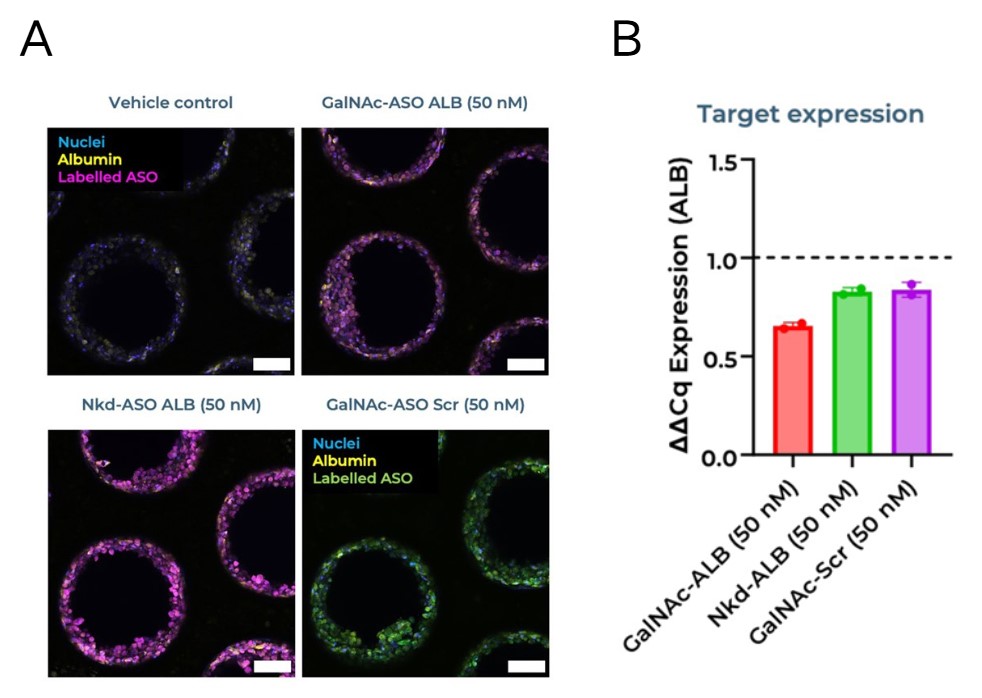
图4.单次给药下反义寡核苷酸的持续摄取和有效基因靶向。(A)固定后的免疫荧光成像显示Cy5标记反义寡核苷酸(品红色)、细胞核(蓝色)、白蛋白(黄色)和FAM标记非靶向反义寡核苷酸(绿色)的摄取。(B)在单次给予50nM浓度后,与其他条件相比,GalNAc-ALBASO对ALB基因的敲低效果更大。比例尺:100μm。
结果五:在肝脏MPS中比较GalNAc偶联、荧光标记反义寡核苷酸的单次和重复给药
接下来,我们旨在研究在14天周期内,单次给药(第4天)或重复给药(第4、6和8天)这两种给药策略的效果。我们发现不同治疗方案间的乳酸脱氢酶和白蛋白结果相当;在比较所使用的三种不同反义寡核苷酸时,结果也相似(图5A-B)。无论在单次给药还是重复给药中,与Nkd-ALBASO相比,GalNAc-ALBASO对ALB基因表达的敲低均更大(图3C-D)。与重复给药导致更大基因敲低的结果一致,我们观察到,与单次给药相比,重复给药中靶向白蛋白基因和乱序对照的反义寡核苷酸的摄取均更多(图5E-F)。这凸显了肝脏MPS能够促进重复给药的能力,而这在新药物模式的临床应用中通常是常态。

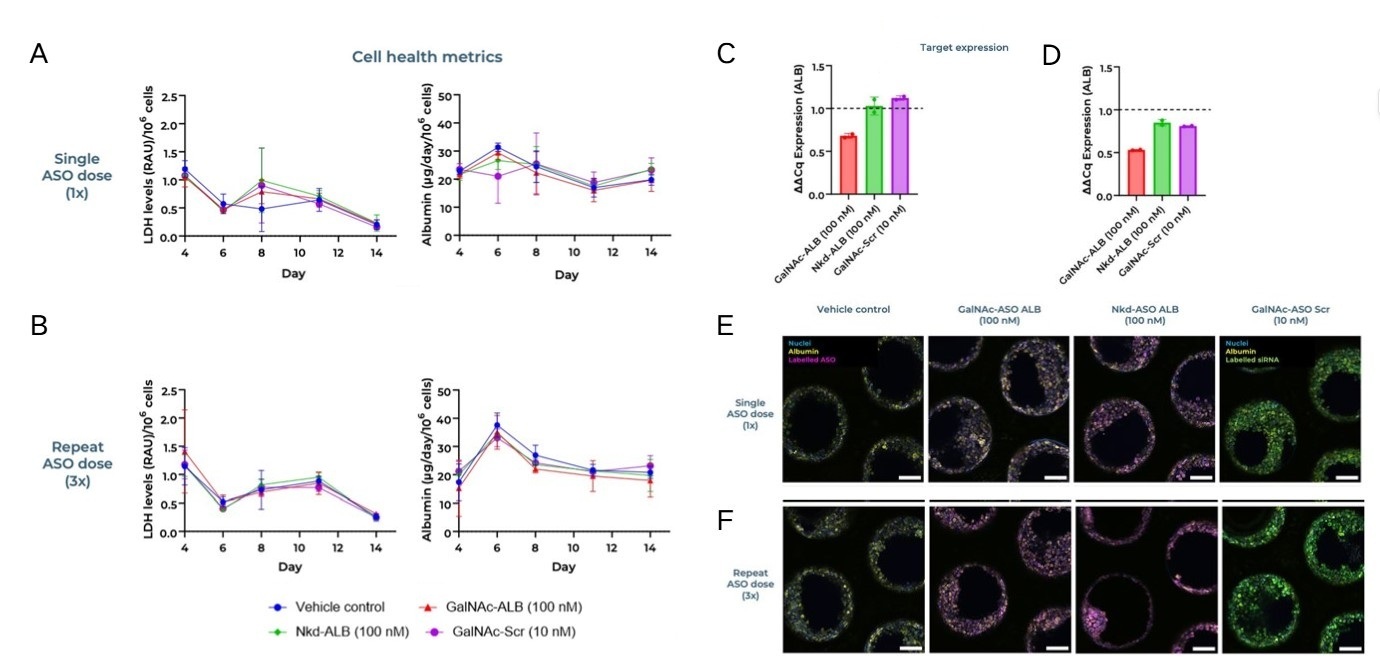
图5.在肝脏MPS中比较GalNAc偶联、荧光标记反义寡核苷酸的单次和重复给药。原代人肝细胞在14天周期内,用靶向白蛋白基因表达的反义寡核苷酸处理一次(单次;第4天)或三次(重复;第4、6、8天)。在(A)单次和(B)重复给药条件下,为期14天的实验中,低乳酸脱氢酶和稳定的白蛋白水平表明细胞健康。在(C)单次和(D)重复给药条件下,GalNAc偶联靶向ALB的反义寡核苷酸、非偶联靶向ALB的反义寡核苷酸以及GalNAc偶联非靶向反义寡核苷酸的基因表达情况。免疫荧光成像显示在(E)单次和(F)重复给药条件下的细胞核(蓝色)、白蛋白(黄色)、Cy5标记靶向反义寡核苷酸(品红色)和FAM标记非靶向反义寡核苷酸(绿色)。比例尺:100μm。
四、讨论分析:肝脏MPS在寡核苷酸摄取与基因敲低中的应用价值
在这项研究中,我们展示了肝脏MPS在检测靶向肝脏的寡核苷酸的摄取和基因敲低方面的有效性。我们使用了靶向GAPDH基因的小干扰RNA和靶向ALB基因的反义寡核苷酸。对于每种模式,我们都包含了一个非编码乱序对照,以评估无基因靶向时的细胞摄取。我们的结果显示,单次给药时,我们的系统能有效摄取小干扰RNA和反义寡核苷酸,且重复给药时摄取增加。与非偶联模式相比,GalNAc偶联的小干扰RNA和反义寡核苷酸分别对其目标基因GAPDH和ALB有更大的敲低效果。
其他团队更近的研究利用我们肝脏MPS中的原代人肝细胞,探索了反义寡核苷酸的细胞摄取情况(Majeretal.,2024)。Majer等人利用多光子成像证明,与Nkd-反义寡核苷酸相比,GalNAc-反义寡核苷酸在1小时时的摄取增加。然而,在4小时时,观察到相反的情况,即用Nkd-反义寡核苷酸处理的原代人肝细胞中,信号强度(标记的反义寡核苷酸)高于GalNAc偶联的反义寡核苷酸。作者还区分了立方体形和非立方体形的肝细胞,并检测了被内吞的反义寡核苷酸的运输过程。他们发现,在立方体形肝细胞中,细胞内脂质与被内吞的反义寡核苷酸不存在共定位现象。未来的研究可以调查一种剂量-反应测定,采用更少的处理次数但使用更高浓度的新药物模式。此外,为了研究GalNAc对其肝细胞上受体的特异性,可以引入另一种细胞类型,例如Kupffer细胞,以证明在我們的系统中使用GalNAc偶联模式时对原代人肝细胞的偏好性。纳入Kupffer细胞也有助于检测寡核苷酸的任何免疫驱动毒性,因为这些细胞是肝脏中驻留的巨噬细胞群体的一部分。
五、结论与展望:肝脏芯片用于寡核苷酸疗法体外筛选
我们的研究证明了原代人肝脏MPS和寡核苷酸递送测定在克服非人模型局限性方面的实用性,可用于评估靶向肝脏的寡核苷酸的摄取和基因敲低效力。使用PhysioMimix Core系统和多芯片肝脏-12板,我们得以在3D胶原蛋白涂层支架上生成稳定且有功能的人体肝脏组织,用于测试小干扰RNA和反义寡核苷酸。我们的结果显示,单次给药时,小干扰RNA和反义寡核苷酸均能被有效摄取,且重复给药时摄取增加。值得注意的是,与未偶联模式相比,GalNAc偶联的小干扰RNA和反义寡核苷酸分别对目标基因GAPDH和ALB表现出更大的敲低效果。这些发现凸显了PhysioMimix肝脏MPS在体外测试新型治疗模式方面的潜力,并强调了给药策略在实现功能性基因敲低中的重要性。我们未观察到蛋白质水平的敲低效应。给药可能本会达到一个KD值,进而在细胞功能方面产生下游响应,但在此处我们给药剂量过轻。肝脏组织细胞仍保持靶向性,但仍具活力。基于肝脏MPS的寡核苷酸测定提供了一种稳健的生理学方法,可在初次人体试验前进行寡核苷酸疗法的测试,并可作为动物体内模型的替代方案。
本文基于CN Bio官方公开研究资料由其中国供应商上海曼博生物整理,仅用于科研信息分享。上海曼博生物可提供完整的器官芯片实验解决方案及相关产品技术支持(https://www.mine-bio.com/CN-Bio-Innovations/Physiomimix.shtml)。
文献参考
[1] J.Debackeretal.,(2020).Mol.Ther.28(8):1759-1771
[2] K.J.Livak&T.D.Schmittgen(2001),Methods.25(4):402-408
[3] J.Majeretal.,(2024).Lab.Chip.24(19):4594-4608
[4] T.C.Robertsetal.,(2020).Nat.Rev.DrugDiscov.19(10):673-694
[5] Rubianoetal.,(2021).Clin.Transl.Sci.14(3):1049-1061
扩展阅读
2.CNBio微流控器官芯片系统|在多种MPS中领跑胆汁淤积性DILI预测:https://www.mine-bio.com/CNBIO-Article/CN-BIO-Article-38.shtml


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 















