
 发布时间:2026/04/14 点击数:254
发布时间:2026/04/14 点击数:254 LifeNet Health|人原代肝细胞3D肝球体标准化培养实操方案
摘要
针对3D肝球体传统培养中形态不均、功能维持时间短、实验重复性差的技术痛点,本文详细阐述LifeNet Health基于人原代肝细胞的3D肝球体培养标准化方案,包含培养基制备、细胞复苏接种、培养维护全流程实操参数,及配套产品选型、模型应用场景,为肝脏相关体外研究提供可复现的技术参考。
如何通过标准化操作构建形态均一、功能稳定的人原代肝细胞3D肝球体,解决传统培养流程中操作不统一、实验数据不可重复的技术难题?
一、3D肝球体培养的核心技术痛点与标准化方案设计思路
3D肝球模型可复刻体内肝细胞的空间结构与细胞间交互作用,是肝脏疾病机制、药物代谢评估的重要体外工具,传统培养模式因缺乏统一操作规范,易出现肝球形成大小不均、肝细胞功能快速衰减、不同实验室数据无法复现等问题。
本方案基于40余年人原代肝细胞研究经验,从培养全流程关键参数控制入手,制定标准化操作规范,搭配适配的细胞、培养基及耗材,实现3D肝球体的稳定培养,保障实验结果的一致性与可重复性。
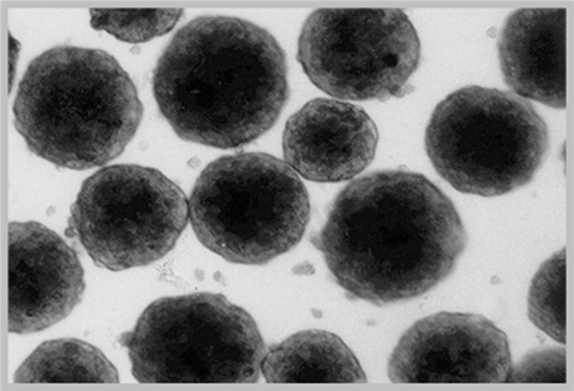
图1:人原代肝细胞球体形成
二、3D肝球体培养三步标准化实操流程
本方案围绕培养基制备、细胞复苏与接种、培养与维护三个核心环节制定操作标准,可直接落地应用,具体操作如下:
2.1 培养基制备:预混配方+无菌操作规范
方案配套三款专用培养基,采用预混补充剂设计,减少人工配比误差,配制全程遵循无菌操作要求,具体配方与操作:
铺板培养基(HHPM):250mL基础培养基中添加15mL专用补充剂(HHPMS),按需添加青霉素/链霉素,70%酒精消毒后在生物安全柜内完成配制;
维持培养基(HHCM):500mL基础培养基搭配5mL补充剂(HHCMS),配制后经0.2μm滤膜过滤灭菌,4℃保存备用;
复苏培养基(HHTM):使用前充分倒置混匀,37℃水浴预热20-30分钟,为细胞复苏提供合适的渗透压与温度环境。
2.2 细胞复苏与接种:分步控温+适配接种密度
人原代肝细胞对温度与机械操作敏感,复苏阶段采用分步控温+温和解冻策略,接种密度严格量化,保障细胞活性与成球均一性,操作要点:
冻存管转运:从液氮罐取出冻存管后,立即放入盛有液氮的便携容器,避免运输过程中温度回升;
水浴解冻:37℃恒温水浴中垂直放置冻存管,仅细胞悬液部分浸入水中,90秒内完成解冻;需倒置检查悬液流动性——未完全液化者仅追加5秒水浴,避免过度解冻损伤细胞;
细胞接种:推荐15,000 cells/mL、30,000 cells/mL两种接种密度,对应96孔板每孔1,500 cells、3,000 cells,采用多通道移液器分注100μL细胞悬液,保证每孔细胞量一致。
按此流程操作,人原代肝细胞复苏存活率≥80%,可形成直径150-200μm的均一肝球体,球体边缘光滑、内部细胞排列紧密。
2.3 培养与维护:静置成球+半量换液策略
3D肝球体形成与功能维持的关键为减少外部干扰+平衡营养供给,采用静置培养结合半量换液的方式,具体操作:
静置成球:细胞接种后前5天全程静置培养,让细胞自然聚集形成球体,避免早期操作破坏球状体结构;
半量换液:第5天进行头次换液,用37℃预热的完全HHCM更换50μL孔内培养基,避免剧烈操作打散球体;后续每48小时(周一、三、五)半量换液一次;
培养周期:推荐连续培养21天,可保障肝球体的形态与功能稳定性。
图2:肝球体形成的图像
(A)单个聚集体正在形成,但无法聚结为单个球体(B)聚集体正在形成,但边缘不光滑,类球体颜色较深(C-D)良好、致密、半透明的类球体,边缘清晰可辨。
三、3D肝球体培养配套产品选型与技术要求
3D肝球体的稳定形成依赖细胞、培养基、耗材的协同适配,各配套产品需满足以下技术要求,避免因产品不兼容导致实验失败:
人原代肝细胞:LifeNet Health冻存人原代肝细胞复苏活性高,具备出色的聚集成球能力,具备自然聚集成球能力,无需额外驯化即可用于3D培养;
专用培养基:复苏、铺板、维持三款培养基均针对人原代肝细胞3D培养优化,含肝细胞生长所需的特异性因子,保障肝细胞功能维持;
培养耗材:选用低吸附U型底96孔板,减少细胞贴壁干扰,引导细胞向中心聚集,保障肝球体形态均一。
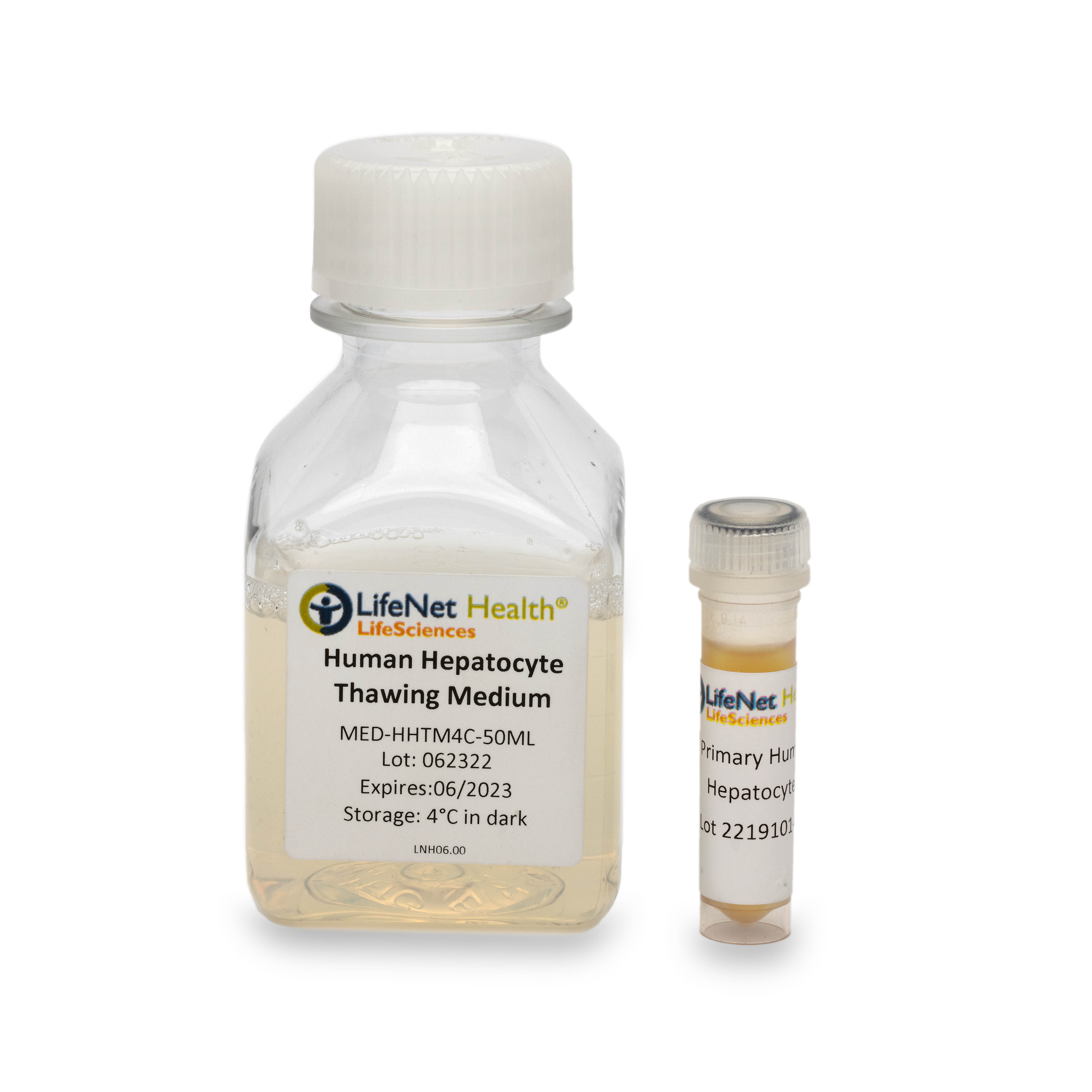
图3:人原代肝细胞与原代肝细胞复苏培养基
四、人原代肝细胞3D肝球体的核心应用场景
本方案构建的3D肝球体可高度模拟体内肝细胞的生理状态与功能,适用于肝脏领域多种体外研究场景,具体包括:
肝脏疾病机制研究:采用NASH、肝纤维化等疾病供体的人原代肝细胞构建3D肝球模型,复刻体内肝脏病理状态,解析疾病发生发展机制;
药物代谢与肝毒性评估:模拟药物在体内的长期暴露效应,检测药物代谢规律、代谢产物生成,及药物对肝细胞的潜在毒性作用;
环境与食品毒理学研究:评估环境污染物、食品添加剂等外源性物质对肝脏的损伤作用,为食品安全与环境健康评估提供实验数据。
总结
LifeNet Health标准化方案通过对人原代肝细胞3D肝球体培养全流程的关键参数进行量化与规范,解决了传统培养中形态不均、功能维持短、实验重复性差的技术痛点。从培养基预混配方、细胞分步控温复苏,到静置成球+半量换液的培养维护,所有操作均具备明确的技术指标,可直接落地应用。
配套的细胞、培养基与耗材经协同验证,进一步提升了3D肝球体培养的稳定性,构建的肝球模型可贴合体内肝细胞生理状态,适用于肝脏疾病机制、药物代谢与毒性评估、毒理学研究等多个领域,为肝脏相关体外研究提供了可复现、高可靠的技术方法。
FAQ:人原代肝细胞3D肝球体培养常见技术问题
Q1:如何选择合适的人原代肝细胞批次?
A1:选择复苏活率高、成球能力好、COA 质控齐全合格的细胞批次,优先选用经 3D 培养验证的 LifeNet Health 原代肝细胞。
Q2:按本方案操作,人原代肝细胞的复苏存活率可达多少?
A2:复苏存活率以细胞批次COA 标注值为准;严格按方案规范操作,可使实际活率达到或接近 COA 标准水平,并形成 150–200 μm 均一肝球体。
Q3:3D肝球体培养过程中,为何前5天需要全程静置?
A3:前5天是细胞自然聚集形成球体的关键阶段,静置培养可避免液体晃动、换液等操作对细胞聚集状态的破坏,保障肝球体正常形成。
Q4:本方案中半量换液的核心优势是什么?
A4:半量换液可在保障肝细胞获得新鲜营养的同时,保留孔内部分原有培养基,平衡营养供给与代谢废物清除,且避免全量换液导致的肝球体结构打散。
Q5:推荐使用什么培养板培养肝球体?
A5:建议使用超低吸附 U 型底 96 孔板,减少贴壁并利用重力引导细胞向中心聚集,提升成球均一性。。
Q6:本方案构建的3D肝球体可稳定培养多久?
A6:按每48小时半量换液的维护方式,3D肝球体可连续稳定培养21天,期间肝细胞形态与功能均能保持稳定。
Q7:接种密度推荐多少?
A7:96 孔板推荐两种密度:每孔1500 cells或3000 cells,对应悬液浓度 15,000 cells/mL 或 30,000 cells/mL。
Q8:细胞复苏为何要严格控制时间、避免过度解冻?
A8:原代肝细胞对温度敏感,过度解冻会显著降低活力;严格控制时间解冻可最大程度保护细胞活性。
技术支持说明
本3D肝球体培养标准化方案由LifeNet Health研发,该机构长期专注于人原代肝细胞相关研究与体外实验技术开发,拥有完善的人源细胞研究体系。上海曼博生物医药科技有限公司为LifeNet Health中国大陆地区官方供应商,直售人原代肝细胞及配套肝细胞培养基(https://www.mine-bio.com/LifeNet_PrimaryCells_Medium/)。若需了解实验方案细节,可联系曼博生物技术团队,获取专属技术支持。


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 














