
 发布时间:2026/06/04 点击数:257
发布时间:2026/06/04 点击数:257 深度解读:一文解锁LifeNet Health人原代肝细胞白皮书核心要点
本文摘要:本文详解LifeNet Health人原代肝细胞生理特性、应用、制备质控与分型,为药物研发提供高可靠体外模型,可咨询中国区供应商曼博生物了解人肝细胞技术详情。
以下内容基于LifeNet Health人原代肝细胞白皮书整理,如需了解更多详情,您可点击获取曼博生物肝细胞技术支持。
一、人原代肝细胞核心生理特性
1.1 肝细胞基础生理特征
在健康成人肝脏中,肝细胞占肝脏总体积的80%、细胞总数的60%,为高度极化的上皮细胞,可执行肝脏核心生化与生理功能,包括合成白蛋白、中甲状腺素结合球蛋白等血液结合/载体蛋白,及合成外源性物质摄取、代谢、外排相关的代谢酶与转运蛋白。
1.2 肝小叶分区的功能差异性
肝小叶可分为门静脉周围区(1区)、小叶中区(2区)、中心周围区(3区),因微血管分布、血流定向性形成的自然梯度与微环境,导致不同区域肝细胞的基因表达、表型及功能存在明显差异:
1区肝细胞的脂肪酸β-氧化、胆固醇代谢能力及PPAR调节基因表达更为突出;
2区中间过渡带,功能为 1区 和 2区的混合;3区肝细胞的胆汁酸、脂肪生成及谷氨酰胺合成酶代谢能力更强,且参与外源物生物转化的多数细胞色素P450(CYP)酶在此区域表达水平更高;
3区肝细胞同时高表达OATP1B1、OATP1B3等摄取转运蛋白与CYP蛋白,具备完善的外源物蓄积与代谢能力,也更易受CYP介导的活性代谢物相关毒性影响;
不同肝小叶区域对肝毒性物质的反应存在特异性,如对乙酰氨基酚易引发3区毒性,烯丙醇、磷则易导致1区特异性损伤。
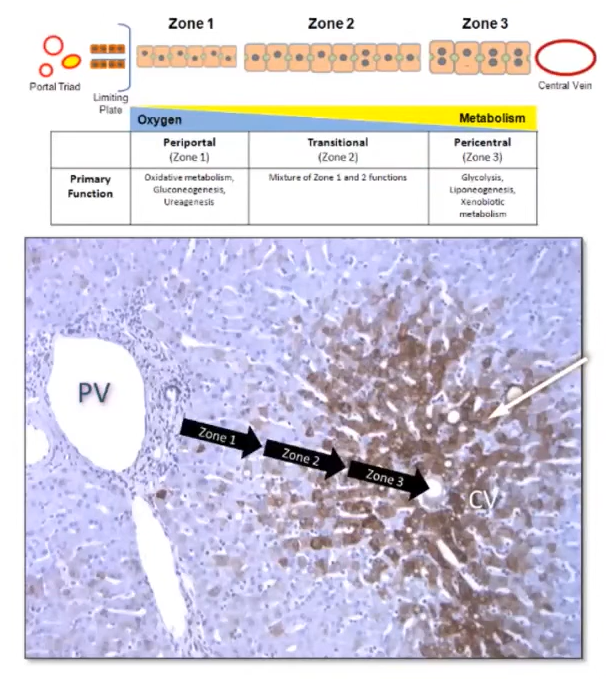
图1. 肝小叶分区图(PV:Portal Vein肝门静脉;CV:Central Vein中央静脉)。注:图示来源LifeNet Health 官方Webinars
二、人原代肝细胞在ADMET领域的核心应用
人原代肝细胞构建的体外模型是评估新化学物质代谢、酶诱导潜力的金标准,在药物研发的ADMET(吸收、分布、代谢、排泄、毒性)研究中具有重要价值,不同培养体系的适配场景如下:
悬浮培养体系:可成功预测化合物体内药代动力学及清除率,是药物发现早期阶段评估代谢稳定性与代谢途径的常用核心方法;
三明治培养(SC)体系:可评估化合物通过诱导/抑制肝酶引发的不良反应风险,同时能有效研究药物摄取/外排转运体功能,预测化合物的胆汁分泌及代谢产物生成;
三维(3D)球体培养体系:提升体外模型的生理相关性,可维持肝细胞高代谢稳定性并实现长期体外培养,能检测到二维(2D)单层培养无法观测的体内肝脏毒性,大幅提升药物性肝损伤(DILI)预测的准确性;
长效代谢稳定培养体系:适用于低代谢率药物的长期清除过程研究,同时为药物代谢、转运及DILI的体外研究提供更贴合体内生理状态的实验模型。
此外,人原代肝细胞体外模型可实现候选药物肝毒理机制的高通量快速筛选,能评估活性代谢产物的蛋白质加合、线粒体功能紊乱、外排转运蛋白抑制等DILI关键诱因,且在补充胆汁酸的条件下,检测结果与临床结果的一致性更高。
三、人原代肝细胞分离制备技术
3.1 传统肝细胞分离方法及其局限性
目前人原代肝细胞的分离多基于经典两步法,依赖粗制胶原酶与非特异性蛋白酶制剂,且普遍采用Percoll密度梯度离心富集,所得细胞批次因混有不同比例肝小叶分区亚群及非实质细胞(NPCs),存在组成与表型的明显差异,影响实验重复性。
3.2 肝细胞制备技术优化点
LifeNet Health人原代肝细胞在标准化的采集条件下制备,核心优化点体现在:
从组织采集到实验室转运全程采用增强型组织灌流与保存技术,尽可能缩短热缺血/冷缺血时间;
将超过35年的临床产品生产、质控体系延伸至临床前组织与细胞产品,建立更高标准的采集与监测体系,提升了组织处理的整体成功率及肝细胞制备质量。
四、冻存人原代肝细胞包含哪些质控项目?
LifeNet Health每批次冻存人原代肝细胞均配备全面的质检报告(CoA),并经过多维度的功能与质量表征,质控体系覆盖人口统计学、病理检测、基因分型、酶活性检测等全维度,核心质控项目如下:
基础信息与病理检测:包含捐赠者人口统计学数据、血液生化指标、BMI指数、药物/酒精/烟草接触史、血清学检测结果;所有组织样本经委员会认证病理学家进行NAFLD活动度评分,CoA附组织病理学评分及H&E、三色染色图像;
图2.脂肪肝组织病理学图像(三色染色),白色箭头指示脂滴。
药理基因分型:完成与候选药物代谢直接相关的I相、II相酶基因分型,包含实际测序结果、参考等位基因及112个单核苷酸多态性(SNP)的等位基因频率,并按捐赠者种族进行定制化分析,可将个体分为弱代谢型、中间代谢型、强(正常)代谢型;
细胞基础特性检测:确定细胞复苏后的平均存活率、产量、形态完整性、贴壁效率,明确适配的培养类型;贴壁型批次标注恰当的接种密度,CoA附单层细胞培养代表性图像;
CYP酶活性检测:使用阳性选择性底物测定CYP1A2、CYP2B6、CYP2C9、CYP2C8、CYP2C19、CYP3A4的活性;评估7-乙氧基香豆素(7-EC)、7-羟基香豆素(7-HC)经I相、II相代谢酶生成代谢产物及硫酸化/葡糖醛酸耦合物的能力;
酶诱导响应检测:中/长期贴壁肝细胞经48/72小时诱导处理后,检测CYP1A2/2B6/3A4对原型诱导剂的响应,报告mRNA表达倍数及特异性酶活性数据。
五、为什么选择LifeNet冻存人原代肝细胞?其分型可用于哪些应用场景?
完成复苏检测后,LifeNet Health冻存人原代肝细胞按应用场景进行标准化分类,各分型均经过上述全维度质控,且CoA配套对应专属检测数据与图像,核心分型及适配场景如下:
5.1 成人悬浮型/短期贴壁型
核心应用:新药研发早期评估新化合物的代谢稳定性、代谢途径,推算生物利用度、半衰期等药代动力学参数,是该研究场景的金标准材料;
质控特点:经全套CYP酶活性检测及7-EC/7-HC代谢能力评估,CoA包含复苏存活率、单支产量及对应培养条件下的代表性图像。
图3. 成人原代肝细胞,复苏后(明场)
5.2 成人中期/长期贴壁型
核心应用:评估体内药物相互作用的潜在风险,检测新化学实体(NCE)对I/II相代谢酶、摄取/外排清除机制的上调作用;适配三维(3D)球体培养体系以提升体外模型生理相关性;支撑低代谢率药物的长期清除过程研究,为临床用药方案与药物代谢研究提供可靠依据
质控特点:完成奥美拉唑(CYP1A2)、苯巴比妥(CYP2B6)、利福平(CYP3A4)等核受体通路阳性诱导剂的测试,提供48/72小时诱导后的mRNA表达及酶活性数据;CoA附推荐接种密度,中期贴壁型附5天单层培养图像(图3a),长期贴壁型附10天单层培养图像(图3b);所有批次保证稳定培养至少1周,且诱导性能达标。


图4.成人原代肝细胞贴壁图像。上图:a)贴壁120 h单层培养图像(100X);下图:b)贴壁240 h单层培养图像(100X)
5.3 成人高BMI/NAFLD/NASH型
核心应用:研究NAFLD/NASH疾病状态下的药物代谢酶(DMEs)与转运蛋白表达变化,发现肝病新药靶点,解析NAFLD/NASH患者群体的药物清除与毒理机制,评估药物在肝病模型中的安全性与有效性;
质控特点:涵盖脂肪变性、NASH、肝细胞癌(HCC)等不同阶段的NAFLD捐赠者肝细胞,经病理学家对组织切片进行组织病理学评价;采用专属采集分离流程制备,经贴壁性能与功能验证,CoA附H&E、三色染色图像及病理评分。
5.4 新生儿/儿童/青少年型
核心应用:研究药物代谢及清除机制的年龄依赖性差异,探究不同年龄段的肝毒性反应潜在风险,为新生儿、儿童群体的药物研发提供贴合生理状态的实验模型;
质控特点:覆盖新生儿(<2个月)、儿童(1-12岁)、青少年(13-18岁)全年龄段,经全套CYP酶活性及代谢能力检测;CoA包含捐赠者信息、复苏数据、推荐接种密度及对应培养条件下的代表性图像。
注:各分型均提供悬浮型/贴壁型两种形式,可满足不同培养体系的实验需求。
六、总结
LifeNet Health人原代肝细胞依托专属的组织采集与制备技术,解决了传统分离方法导致的细胞表型不均问题,同时建立了覆盖病理、基因、酶活性、诱导响应的全维度质控体系,每批次产品均配备信息完整的CoA,保障了实验的可重复性与数据的可靠性。
FAQ:LifeNet Health人原代肝细胞产品核心问题
Q1:什么是人原代肝细胞?它的主要组成和核心价值是什么?
A1:人原代肝细胞是从人肝脏组织中直接分离获取的原代肝细胞,可分为肝实质细胞(primary hepatocytes)和肝非实质细胞,其中肝实质细胞是原代肝细胞中最主要的组成部分,占肝脏体积约80%、细胞总数60%,具备肝脏完整生理代谢、解毒、合成功能,是体外药物研究的金标准模型。
Q2:肝小叶分区(1/2/3区)对肝细胞功能有何影响?
A2:1区(门静脉周围):脂肪酸氧化、胆固醇代谢强,毒性敏感性低;2区(小叶中区):功能过渡区域;3区(中心周围):CYP450酶表达最高,外源物代谢强,更易发生肝毒性
Q3:为什么原代肝细胞比肝癌细胞系更可靠?
A3:原代肝细胞保留完整代谢酶、核受体、转运蛋白与生理调控通路,结果更贴近临床;细胞系基因与表型突变,代谢功能大幅丢失。
Q4:为什么需要新生儿/儿童肝细胞?
A4:药物代谢酶与转运体随年龄发育,儿童与成人药代/毒理差异显著,该模型用于儿科药物研发与剂量设计。
Q5:LifeNet Health人肝细胞的供体来源是否合规?
A5:LifeNet Health作为美国联邦指定的器官获取组织(OPO),所有供体均经伦理审批、知情同意,完成全套传染病筛查与肝脏病理评估,完全符合国际生物样本伦理与合规要求,可用于药物研发等合规实验。
Q5:冻存肝细胞复苏后如何判断质量合格?
A5:合格标准为:细胞存活率≥70%-80%,贴壁均匀、细胞形态完整无大量碎片。
上海曼博生物为LifeNet Health人原代肝细胞中国区官方供应商,可为国内科研机构提供本产品的技术咨询、产品配套及售后支持服务,如需获取人原代肝细胞产品详细信息可点击此处咨询曼博生物!
拓展阅读
参考文献
1. Bioulac-Sage, P., LeBail, B. and Balabaud, C. Liver and biliary tract histology, In:Rodes, J., Benhamou, J.-P., Blei, A. T., Reichen, J. & Rizzetto, M. (eds.)Textbook of Hepatology:From Basic Science to Clinical Practice, 3rd Edition.Malden:Wiley Blackwell Publishing, 2007
2. Kmiec, Z. Cooperation of liver cells in health and disease.Adv Anat Embryol Cell Biol, 161, Iii-xiii, 1-151, 2001.
3. Klaassen, C. D., Casarett, L. J. and Doull, J. Casarett and Doull’s toxicology the basic science of poisons.McGraw-Hill Medical Pub, 2013.
4. Rodes, J. Textbook of hepatology : from basic science to clinical practice, 3rd Edition.Malden, Mass., Blackwell, 2007.
5. Ito, Y. and McCuskey, R. Hepatic microcirculation In:Rodes, J., Benhamou, J., Blei, A., Reichen, J. and Rizzetto, M. (eds.)Textbook of Hepatology:From Basic Sciences to Clinical Practice.3rd Ed. Malden Wiley-Blackwell Publishing, 2007
6. Rappaport, A. M. Microcirculatory units in the mammalian liver.Their arterial and portal components.Bibl Anat, 116-20, 1977.
7. Smith, M. T. and Wills, E. D. Effects of dietary lipid and phenobarbitone on the distribution and concentration of cytochrome P-450 in the liver studied by quantitative cytochemistry.FEBS Lett, 127:33-6, 1981.
8. Ugele, B., Kempen, H. J., Kempen, J. M., Gebhardt, R., Meijer, P., Burger, H. J. and Princen, H. M. 1991.Heterogeneity of rat liver parenchyma in cholesterol 7 alpha-hydroxylase and bile acid synthesis.Biochem J, 276 ( Pt 1):73-7, 1991
9. Gebhardt, R. and Matz-Soja, M. Liver zonation:Novel aspects of its regulation and its impact on homeostasis.World J Gastroenterol, 20:8491-504, 2017.
10 LeCluyse, E. L., Witek, R. P., Andersen, M. E. and Powers, M. J. Organotypic liver culture models: meeting current challenges in toxicity testing.Crit Rev Toxicol, 42:501-48, 2012.
11. Wojcik, E., Dvorak, C., Chianale, J., Traber, P. G., Keren, D. and Gumucio, J. J. Demonstration by in situ hybridization of the zonal modulation of rat liver cytochrome P-450b and P-450e gene expression after phenobarbital.J Clin Invest, 82:658-66, 1988.
12. Badr, M. Z., Belinsky, S. A., Kauffman, F. C. and Thurman, R. G. Mechanism of hepatotoxicity to periportal regions of the liver lobule due to allyl alcohol: role of oxygen and lipid peroxidation.J Pharmacol Exp Ther, 238:1138-42, 1986.
13. Przybocki JM, Reuhl KR, Thurman RG, Kauffman FC.Involvement of nonparenchymal cells in oxygen-dependent hepatic injury by allyl alcohol. Toxicol Appl Pharmacol.115(1):57-63, 1992.


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 














